
 £©µÄĖµ·ØÕżČ·µÄŹĒ£®
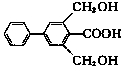
£©µÄĖµ·ØÕżČ·µÄŹĒ£®| A£® | ·Ö×ÓŹ½ĪŖC15H19O4 | |
| B£® | ±½»·ÉĻµÄŅ»ĀČ“śĪļÓŠ7ÖÖ | |
| C£® | ÄÜ·¢ÉśŃõ»Æ·“Ó¦ŗĶČ”“ś·“Ó¦ | |
| D£® | 1molXÓė×ćĮæµÄNaOHČÜŅŗ·“Ó¦£¬×ī¶ąĻūŗÄ3molNaOH |
·ÖĪö Óɽį¹¹æÉÖŖ·Ö×ÓŹ½£¬·Ö×ÓÖŠŗ¬-OH”¢-COOH£¬±½»·ÉĻŗ¬4ÖÖH£¬½įŗĻ“¼”¢ōČĖįµÄŠŌÖŹĄ“½ā“š£®
½ā“š ½ā£ŗA£®Óɽį¹¹æÉÖŖ£¬·Ö×ÓŹ½ĪŖC15H14O4£¬¹ŹA“ķĪó£»
B£®±½»·ÉĻŗ¬4ÖÖH£¬±½»·ÉĻµÄŅ»ĀČ“śĪļÓŠ4ÖÖ£¬¹ŹB“ķĪó£»
C£®ŗ¬-OHæÉ·¢ÉśČ”“ś”¢Ńõ»Æ·“Ó¦£¬ŗ¬-COOHæÉ·¢ÉśČ”“ś·“Ó¦£¬¹ŹCÕżČ·£»
D£®Ö»ÓŠ-COOHÓėNaOH·“Ó¦£¬Ōņ1molXÓė×ćĮæµÄNaOHČÜŅŗ·“Ó¦£¬×ī¶ąĻūŗÄ1molNaOH£¬¹ŹD“ķĪó£»
¹ŹŃ”C
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄ½į¹¹ÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ¹ŁÄÜĶÅÓėŠŌÖŹµÄ¹ŲĻµ”¢ÓŠ»ś·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā“¼”¢ōČĖįµÄŠŌÖŹ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øıäĢõ¼žĒ°ŗó£¬BµÄ×Ŗ»ÆĀŹ¾łĪŖ40% | |
| B£® | øıäĢõ¼žĒ°ŗó£¬CµÄ·“Ó¦ĖŁĀŹ±£³Ö²»±ä | |
| C£® | Čō±£³ÖĪĀ¶ČŗĶĢå»ż²»±ä£¬ŌŚČŻĘ÷ÖŠŌŁ³äČė1molAŗĶ1molB£¬BµÄ×Ŗ»ÆĀŹ²»±ä | |
| D£® | Čō±£³ÖĪĀ¶ČŗĶĢå»ż²»±ä£¬ŌŚČŻĘ÷ÖŠŌŁ³äČė0.5molB”¢1molCŗĶ1molD£¬BµÄ×Ŗ»ÆĀŹŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| NH3•H2O | 2”Į10-5 |
| HNO2 | 7”Į10-4 |
| HClO | 3”Į10-8 |
| H2CO3 | K1=4”Į10-7 K2=4”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
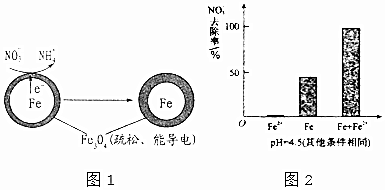
| ³õŹ¼pH | pH=2.5 | pH=4.5 |
| 1Š”Ź±pH | ½Ó½üÖŠŠŌ | ½Ó½üÖŠŠŌ |
| 24Š”Ź±pHNO3-µÄČ„³żĀŹ | ½Ó½ü100% | £¼50% |
| ĢśµÄ×īÖÕĪļÖŹŠĪĢ¬ | 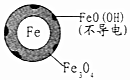 | 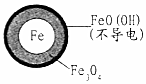 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ÕōøÉCuCl2±„ŗĶČÜŅŗÖʱøĪŽĖ®CuCl2 | |
| B£® | 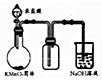 ŹµŃéŹŅÖĘČ”²¢ŹÕ¼ÆÉŁĮæ“æ¾»ĀČĘų | |
| C£® | 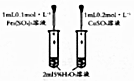 ŃŠ¾æ“߻ƼĮ¶ŌH2O2·Ö½āĖŁĀŹµÄÓ°Ļģ | |
| D£® | 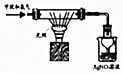 ŃéÖ¤¼×ĶéŗĶŃõĘų¹āÕÕĢõ¼žĻĀ·¢ÉśČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗr£ØZ£©£¾r£ØW£©£¾r£ØY£©£¾r£ØX£© | |
| B£® | YµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČWµÄĒæ | |
| C£® | Z3WÖŠ¼Čŗ¬ÓŠĄė×Ó¼üÓÖŗ¬ÓŠ¹²¼Ū¼ü | |
| D£® | XµÄµ„ÖŹ²»ÄÜÓėYµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ŗĶĻÖĻó | ½įĀŪ |
| A | ĻņĢ¼ĖįÄĘČÜŅŗÖŠ¼ÓČėÅØŃĪĖį£¬½«²śÉśµÄĘųĢåĶØČė±½·ÓÄĘČÜŅŗÖŠ£¬ČÜŅŗ±ä»ė×Ē | ĖįŠŌ£ŗĢ¼Ėį£¾±½·Ó |
| B | Ļņ1mL 0.1mol•L-1 MgSO4ČÜŅŗÖŠ£¬µĪČė2µĪ0.1mol•L-1 NaOHČÜŅŗ£¬²śÉś°×É«³Įµķ£¬ŌŁµĪČė2µĪ0.1mol•L-1CuSO4ČÜŅŗ£¬°×É«³ĮµķÖš½„±äĪŖĄ¶É« | Ksp[Cu£ØOH£©2]£¼Ksp[Mg£ØOH£©2] |
| C | Ļņµ°°×ÖŹČÜŅŗÖŠ¼ÓČė¼×Č©ČÜŅŗŗĶNa2SO4±„ŗĶČÜŅŗ£¬¾ł²śÉś°×É«³Įµķ | µ°°×ÖŹ¾ł·¢ÉśĮĖ±äŠŌ |
| D | ÓĆ²¬ĖæÕŗȔɣĮæijČÜŅŗ½ųŠŠŃęÉ«·“Ó¦£¬»šŃę³Ź»ĘÉ« | øĆČÜŅŗŹĒÄĘŃĪČÜŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬9.2gNO2ĘųĢåÖŠ£®·Ö×ÓŹżĪŖ0.2NA | |
| B£® | pH=2µÄĮņĖįČÜŅŗÖŠ£¬H+ŹżÄæĪŖ0.01NA | |
| C£® | ½«0.05molFeCl3Č«²æ×Ŗ»ÆĪŖFe£ØOH£©3½ŗĢ壬Ōņ½ŗĮ£ŹżÄæĪŖ0.05NA | |
| D£® | 20gD2OÖŠŗ¬ÓŠµÄÖŹ×ÓŹżĪŖ10NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ÓėĻÖĻó | ½įĀŪ |
| A | Ļņµ°°×ÖŹČÜŅŗÖŠµĪ¼ÓPb£ØNO3£©2ČÜŅŗ£¬²śÉś°×É«³Įµķ£¬¼ÓĖ®³Įµķ²»ĻūŹ§ | µ°°×ÖŹ·¢ÉśĮĖ±äŠŌ |
| B | ²ā¶ØÅضČĪŖ 0.1mol•L-1CH3COONaÓėHCOONa ČÜŅŗµÄpH£¬CH3COONaČÜŅŗµÄpH½Ļ“ó | ĖįŠŌ£ŗCH3COOH£¾HCOOH |
| C | ĻņČÜŅŗXÖŠĻȵĪ¼ÓĻ”ĻõĖį£¬ŌŁµĪ¼ÓBa£ØNO3£©2ČÜŅŗ£¬³öĻÖ°×É«³Įµķ | ČÜŅŗXÖŠŅ»¶Øŗ¬ÓŠSO42- |
| D | ĻņÅØ¶Č¾łĪŖ0.1mol•L-1NaClŗĶNaI»ģŗĻČÜŅŗÖŠµĪ¼ÓÉŁĮæ0£®l mol•L-1AgNO3ČÜŅŗ£¬³öĻÖ»ĘÉ«³Įµķ | Ksp£ØAgI£©£¼Ksp£ØAgCl£© |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com