
| A、Ba(OH)2、Na2SO3、FeCl3、KCl |
| B、Na2CO3、NaHCO3、KNO3、NH4Cl |
| C、NH3?H2O、H3PO4、Na2SO4、H2SO4 |
| D、HCl、CH3COOH、C2H5OH、Na2SiO3 |


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
| 反应方程式 | 分析 | |
| A | 回收印刷电路板:Fe3++Cu=Cu2++Fe2+ | 错误,电子得失守恒及电荷守恒未配平 |
| B | 铝投入氢氧化钠溶液:Al+2OH-=AlO2-+H2O | 错误,反应物漏写、产物书写错误 |
| C | SO2通入漂白粉溶液: Ca(ClO)2+SO2+H2O=CaSO3+2HClO | 错误,BaSO3是白色沉淀,应加“↓” |
| D | 氯气通入水中:Cl2+H2O=H++Cl-+HClO | 错误,未写成可逆符号 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原混合物中CuO与Fe2O3物质的量的比为l:l |
| B、反应后所得CO2的质量为8.8g |
| C、参加反应的CO的质量为8.4g |
| D、原混合物中CuO与Fe2O3的质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
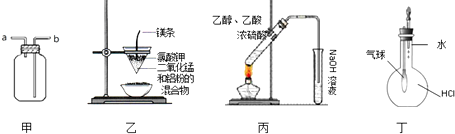
| A、装置甲:气体从a口进入,收集NH3 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B、加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色固体 |
| C、加热时,c中溶液红色变深,冷却后又逐渐变浅 |
| D、水浴时,d内气体颜色加深,e内气体颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHSO4与过量的Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O |
| C、碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com