
ijһ��Ӧ��ϵ�з�Ӧ��������ﹲ���������ʣ�HC1(Ũ)��KMnO4��MnCl2��H2O��Cl2��KCl����֪Cl2��MnCl2Ϊ�����
��1�� �÷�Ӧ�е�������Ϊ____________����������Ϊ________�����������뻹ԭ��������ʵ���֮��Ϊ___________��
��2�� �������������ڱ�״���µ����Ϊ1.12 L����Ӧ������ת�Ƶĵ�����Ϊ_________NA(NA��ʾ�����ӵ���������ֵ)��
��3�� ����Ӧ��ת��0.3 mol���ӣ�������(������)HC1____________g��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017������ʡ������������ѧУ����������ģ�⻯ѧ���������棩 ���ͣ�ѡ����
һ���¶�ʱ����2.0 L�����ܱ������г���2 mol SO2��1 mol O2��������Ӧ��2SO2(g)��O2(g) 2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
2SO3(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0��8 | 1��4 | 1.8 | 1.8 |
����˵����ȷ����( )
A����Ӧ��ǰ2 s �� ƽ������v(O2) �� 0��4 mol��L��1��s��1
ƽ������v(O2) �� 0��4 mol��L��1��s��1
B�����������������䣬���ѹ����1.0 L��ƽ�ⳣ��������
C����ͬ�¶��£���ʼʱ�������г���4 mol SO3���ﵽƽ��ʱ��SO3��ת����С��10%
D�������¶Ȳ��䣬����������ٳ���2 mol SO2��1 mol O2����Ӧ�ﵽ��ƽ��ʱn(SO3)/n(O2)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ�ϰ��ڿ��Ի�ѧ���������棩 ���ͣ������
д�����з�Ӧ�����ӷ���ʽ��
���Ȼ����Һ������������Һ��Ӧ
��ͭƬ����������Ӧ��Һ
��̼�ᱵ�����ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ�ϰ��ڿ��Ի�ѧ���������棩 ���ͣ�ѡ����
���е��뷽��ʽ�У���ȷ����( )
A��Na2SO4=2Na++SO4-2 B��Ba(OH)2=Ba2++ OH-2
C��Al2(SO4)3=2Al3++3SO42- D��Ca(NO3)2=Ca2++2(NO3)2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ�ϰ��ڿ��Ի�ѧ���������棩 ���ͣ�ѡ����
������ԭ��Ӧ��ʵ����( )
A����Ԫ�صĵ�ʧ B�����ϼ۵�����
C�����ӵĵ�ʧ��ƫ�� D��������ԭ�ӵ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ����У��һ�����л�ѧ���������棩 ���ͣ�ѡ����
������ʵ�鷽�����ԴӺ��������������ȡ���п��������Թ��ܵ���Ȼ���

����˵���������
A���������Ҫ����װ�� B���������Ҫ�õ���Һ©��
C���������Ҫ�õ����� D���������Ҫ����װ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ����У��һ�����л�ѧ���������棩 ���ͣ�ѡ����
��������ϵͼ����ȷ����
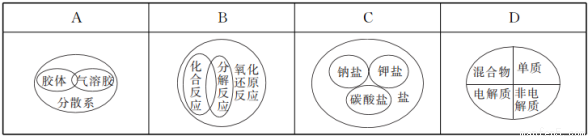
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ɽ�϶��и�����11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ȷ����( )
A������CaCO3������ˮ��ͨ��CO2������ǡ���ܽ⣬������Һ�м���NaHCO3������Һ������CaCO3��������
B����Na2CO3��Һ����μ�������ʵ�����ϡ���ᣬ����CO2��Na2CO3�����ʵ���֮��Ϊ1 ��2
C����������NaHCO3��Na2CO3�ֱ����������ᷴӦ����ͬ��ͬѹ�£����ɵ�CO2�����ͬ
D����Na2CO3������Һ��ͨ��CO2����NaHCO3�ᾧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и������¿��Ļ�ѧ���������棩 ���ͣ�ѡ����
���й�����ͼ��ʾת����ϵ(X����±�أ���˵���������
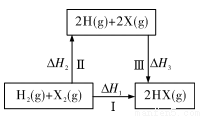
A��2H(g)+2X(g)==2HX(g) ��H3<0
B����H1=��H2+��H3
C��Cl��Br��I�ķǽ��������μ�����������;��I��Ӧ�ġ�H1��С
D��;��I����HC1�ų�������������HBr�Ķ࣬˵��HC1��HBr�ȶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com