
| t/s | 0 | 500 | 1000 |
| C(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
 ;
;| △c |
| △t |
| 1 |
| 2 |
 ,故答案为:
,故答案为: ;
;| 1.48mol/L |
| 500s |
| 1 |
| 2 |


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
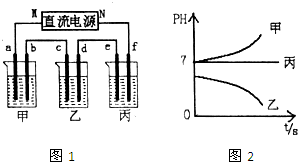
查看答案和解析>>
科目:高中化学 来源: 题型:
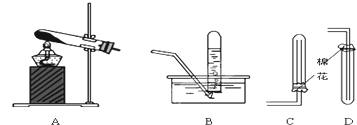
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,y的转化率为75% |
| B、反应可表示为X+3Y?2Z,其平衡常数为1600 |
| C、增大压强使平衡向生成Z的方向移动,平衡常数不变 |
| D、改变温度但不可以改变此反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大反应物浓度,能增大活化分子百分数,所以反应速率增大 |
| B、使用正催化剂,能增大活化分子百分数,所以反应速率增大 |
| C、对于任何反应,增大压强都可加快反应速率 |
| D、升高温度,只能增大吸热反应的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
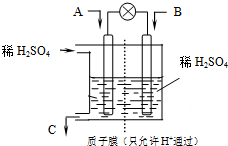 所以“低碳经济”正成为科学家研究的主要课题.
所以“低碳经济”正成为科学家研究的主要课题.| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用500mL容量瓶配制450mL 0.1 moL/L的氢氧化钠溶液,用托盘天平称取氢氧化钠固体1.8g |
| B、用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中 |
| C、用量筒量取浓硫酸时,仰视读数 |
| D、其它环节正确,只是在定容时俯视容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.04mol |
| B、0.03mol |
| C、0.06mol |
| D、0.05mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 待测液 | 消耗标准盐酸(0.01mol?L-1)的体积 | |
| ① | 20mL NaOH溶液 | V1 mL |
| ② | 20mL NaOH溶液+10mL H2O | V2 mL |
| ③ | 敞开隔夜放置的20mL NaOH溶液 | V3 mL |
| A、c=0.01×(V1+V2+V3)/(3×20) |
| B、c=0.01×(V1+V2)/(2×20) |
| C、c=0.01×(V1+V3)/(2×20) |
| D、c=0.01×V1/20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com