
| | ¹ż³ĢIV BČÜŅŗÖŠŗ¬ÓŠµÄĄė×Ó | ¹ż³ĢVI BČÜŅŗÖŠŗ¬ÓŠµÄĄė×Ó |
| ¼× | ÓŠFe3+ĪŽFe2+ | ÓŠSO42© |
| ŅŅ | ¼ČÓŠFe3+ÓÖÓŠFe2+ | ÓŠSO42© |
| ±ū | ÓŠFe3+ĪŽFe2+ | ÓŠFe2+ |
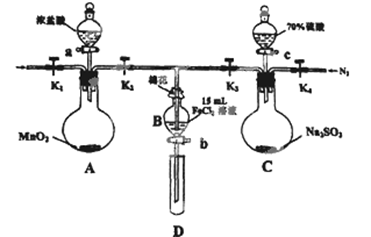
 MnCl2+Cl2”ü+2H2O£»
MnCl2+Cl2”ü+2H2O£» MnCl2 +Cl2”ü+2H2O£»£Ø4£©ÓĆ70£„µÄĮņĖįÖĘČ”SO2£¬·“Ó¦ĖŁĀŹ±ČÓĆ98£„µÄĮņĖįæģ£¬ŹĒŅņĪŖŌŚ98£„µÄĮņĖįÖŠĮņĖįÖ÷ŅŖŅŌ·Ö×ӵĊĪŹ½“ęŌŚ£¬¶ųŌŚ70£„µÄĮņĖįÖŠÓŠ“óĮæµÄĮņĖį·Ö×Ó·¢ÉśµēĄė£¬²śÉśH+£¬¼“70%µÄĮņĖįÖŠµÄH+µÄÅØ¶Č±Č98%µÄĮņĖįÖŠµÄH+µÄÅØ¶Č“ó£»ĖłŅŌĄė×ÓÅضČŌ½“󣬷“Ó¦ĖŁĀŹ¾ĶŌ½æģ”££Ø5£©¹ż³Ģ¢öÖŠ¼ģŃéBČÜŅŗÖŠŹĒ·ńŗ¬ÓŠĮņĖįøłµÄ²Ł×÷·½·ØŹĒȔɣĮæBČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė×ćĮæµÄĻ”ŃĪĖįĖį»Æ£¬ŌŁµĪ¼Ó¼øµĪĀČ»Æ±µČÜŅŗ£¬ČōÓŠ°×É«³ĮµķÉś³É£¬Ö¤Ć÷ČÜŅŗBÖŠÓŠĮņĖįøł”££Ø6£©¼×£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»æÉÄÜÓÉÓŚĀČĘų¹żĮ棬·¢Éś·“Ó¦£ŗCl2£«SO2£«2H2O=SO42-£«4H++2Cl-£»Ö»ÄÜÖ¤Ć÷£ŗŃõ»ÆŠŌ£ŗCl2> Fe3+£»Cl2> SO2”£¶ų²»ÄÜÖ¤Ć÷£ŗFe3 > SO2”£“ķĪó”£ŅŅ£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»2Fe3+£«SO2£«2H2O=SO42-£«4H++2Fe2+£»Ö¤Ć÷Ńõ»ÆŠŌCl2> Fe3+> SO2”£ÕżČ·”£±ū£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»ÓÉÓŚSO2¹żĮ棬ĖłŅŌ·¢Éś·“Ó¦2Fe3+£«SO2£«2H2O=SO42-£«4H++2Fe2+½«ĖłÓŠµÄFe3+»¹ŌĪŖFe2+£»Ö¤Ć÷Ńõ»ÆŠŌCl2> Fe3+> SO2”£ÕżČ·”£Ń”ĻīĪŖŅŅ”¢±ū”£
MnCl2 +Cl2”ü+2H2O£»£Ø4£©ÓĆ70£„µÄĮņĖįÖĘČ”SO2£¬·“Ó¦ĖŁĀŹ±ČÓĆ98£„µÄĮņĖįæģ£¬ŹĒŅņĪŖŌŚ98£„µÄĮņĖįÖŠĮņĖįÖ÷ŅŖŅŌ·Ö×ӵĊĪŹ½“ęŌŚ£¬¶ųŌŚ70£„µÄĮņĖįÖŠÓŠ“óĮæµÄĮņĖį·Ö×Ó·¢ÉśµēĄė£¬²śÉśH+£¬¼“70%µÄĮņĖįÖŠµÄH+µÄÅØ¶Č±Č98%µÄĮņĖįÖŠµÄH+µÄÅØ¶Č“ó£»ĖłŅŌĄė×ÓÅضČŌ½“󣬷“Ó¦ĖŁĀŹ¾ĶŌ½æģ”££Ø5£©¹ż³Ģ¢öÖŠ¼ģŃéBČÜŅŗÖŠŹĒ·ńŗ¬ÓŠĮņĖįøłµÄ²Ł×÷·½·ØŹĒȔɣĮæBČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė×ćĮæµÄĻ”ŃĪĖįĖį»Æ£¬ŌŁµĪ¼Ó¼øµĪĀČ»Æ±µČÜŅŗ£¬ČōÓŠ°×É«³ĮµķÉś³É£¬Ö¤Ć÷ČÜŅŗBÖŠÓŠĮņĖįøł”££Ø6£©¼×£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»æÉÄÜÓÉÓŚĀČĘų¹żĮ棬·¢Éś·“Ó¦£ŗCl2£«SO2£«2H2O=SO42-£«4H++2Cl-£»Ö»ÄÜÖ¤Ć÷£ŗŃõ»ÆŠŌ£ŗCl2> Fe3+£»Cl2> SO2”£¶ų²»ÄÜÖ¤Ć÷£ŗFe3 > SO2”£“ķĪó”£ŅŅ£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»2Fe3+£«SO2£«2H2O=SO42-£«4H++2Fe2+£»Ö¤Ć÷Ńõ»ÆŠŌCl2> Fe3+> SO2”£ÕżČ·”£±ū£ŗ·¢Éś·“Ó¦£ŗ2Fe2++Cl2==2Cl££«2Fe3+£»ÓÉÓŚSO2¹żĮ棬ĖłŅŌ·¢Éś·“Ó¦2Fe3+£«SO2£«2H2O=SO42-£«4H++2Fe2+½«ĖłÓŠµÄFe3+»¹ŌĪŖFe2+£»Ö¤Ć÷Ńõ»ÆŠŌCl2> Fe3+> SO2”£ÕżČ·”£Ń”ĻīĪŖŅŅ”¢±ū”£

 Õć½ĆūŠ£ĆūŹ¦½š¾ķĻµĮŠ“š°ø
Õć½ĆūŠ£ĆūŹ¦½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®µĪ¶ØŹµŃ鏱£¬×¶ŠĪĘæÓĆÕōĮóĖ®Ļ“¾»ŗó£¬Ö±½ÓŹ¢“ż²āŅŗ |
| B£®ÓĆ100mLĮæĶ²ÅäÖĘ100mL0.1000mol?L-1Na2CO3ČÜŅŗ |
| C£®ÓĆ²¬ĖæÕŗȔɣĮæijČÜŅŗ½ųŠŠŃęÉ«·“Ó¦£¬Čō»šŃę³Ź»ĘÉ«£¬ŌņŌČÜŅŗŗ¬ÓŠÄĘŃĪ |
| D£®Ä³ČÜŅŗ¼ÓČėŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³ĮµķÉś³É£¬ŌņŌČÜŅŗŗ¬SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
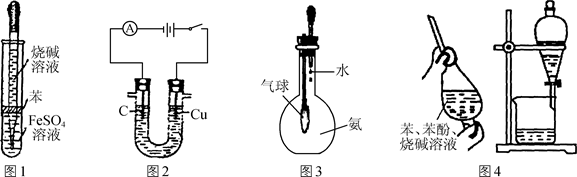
| A£®Ķ¼1ĖłŹ¾×°ÖĆæÉÖʱøĒāŃõ»ÆŃĒĢś |
| B£®Ķ¼2ĖłŹ¾×°ÖĆæɵē½āŹ³ŃĪĖ®ÖĘĀČĘųŗĶĒāĘų |
| C£®Ķ¼3ĖłŹ¾×°ÖĆæÉŃéÖ¤°±Ęų¼«Ņ×ČÜÓŚĖ® |
| D£®Ķ¼4ĖłŹ¾×°ÖĆÓė²Ł×÷æɳżČ„±½ÖŠµÄ±½·Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ö½²ćĪö·Ø½ųŠŠCu2+ŗĶFe3+»ģŗĻŅŗ·ÖĄėŹ±£¬Fe3+ŌŚ¹Ģ¶ØĻąÖŠ·ÖÅä±ČĄż½ĻµĶ |
| B£®ÓƵē×ÓĢģĘ½³ĘĮæ»ÆѧŅ©Ę·Ź±£¬±ŲŠėĻČ³ĘŠ”ÉÕ±µÄÖŹĮ棬ŌŁ³ĘĮæ¼ÓČėŹŌ¼ĮŗóµÄ×ÜÖŹĮ棬Į½ÕßÖ®²ī¼“ĪŖŅ©Ę·µÄÖŹĮæ |
| C£®ŌŚĀĮÓė¹żĮæ3mol”¤L-1ĮņĖįČÜŅŗ·“Ó¦µÄŹŌ¹ÜÖŠ¼ÓČėÉŁĮæNaCl¹ĢĢ壬·“Ó¦ĖŁĀŹ»į¼Óæģ |
| D£®ĪüČėĀČĘų”¢ĀČ»ÆĒāĘųĢåŹ±£¬æÉĪüČėÉŁĮæ¾Ę¾«»ņŅŅĆѵĻģŗĻÕōĘų½ā¶¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

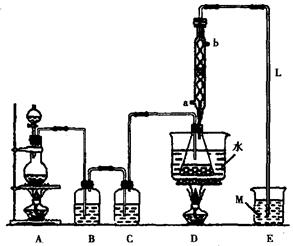
| A£®×°ÖĆ¢ŁÖŠ£¬cĪŖŅõ¼«£¬dĪŖŃō¼« |
| B£®×°ÖĆ¢ŚæÉÓĆÓŚŹµŃéŹŅÕōĮóŹÆÓĶ |
| C£®×°ÖĆ¢ŪÖŠµÄXĪŖCCl4Ź±£¬æÉÓĆÓŚĪüŹÕĀČ»ÆĒāĘųĢ壬²¢·ĄÖ¹µ¹Īü |
| D£®×°ÖĆ¢ÜæÉÓĆÓŚŹÕ¼Æ°±Ęų¼°²¢½ųŠŠĪ²ĘųĪüŹÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
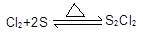
| ŠŌÖŹ ĪļÖŹ | ČŪµć | ·Šµć | ×Å»šµć | ĘäĖūŠŌÖŹ |
| µ„Š±Įņ | 119.2”ę | 446.6”ę | 363”ę | / |
| Š±·½Įņ | 112.8”ę | 446.6”ę | 363”ę | / |
| S2Cl2 | -77”ę | 137”ę | / | ÓöĖ®ĒæĮŅ·Ö½āÉś³ÉS”¢SO2ŗĶHCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĻņÖ󷊵Ä1 mol”¤L£1NaOHČÜŅŗÖŠµĪ¼ÓFeCl3±„ŗĶČÜŅŗÖʱøFe(OH)3½ŗĢå |
| B£®ĻņŅŅĖįŅŅõ„ÖŠ¼ÓČė±„ŗĶNa2CO3ČÜŅŗ£¬Õńµ“£¬·ÖŅŗ·ÖĄė³żČ„ŅŅĖįŅŅõ„ÖŠµÄÉŁĮæŅŅĖį |
| C£®³ĘČ”19.0 g SnCl2£¬ÓĆ100 mLÕōĮóĖ®Čܽā£¬ÅäÖĘ1.0 mol”¤L£1 SnCl2ČÜŅŗ |
| D£®ÓĆĒāŃõ»ÆĶ·ŪÄ©¼ģ²āÄņĢĒ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com