
| A. | ①④ | B. | ③④ | C. | ②③ | D. | ①② |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键.
解答 解:活泼金属和活泼非金属元素之间易形成离子键,有离子键的化合物是离子化合物,
①第3周期第一电离能最小的元素是Na元素、②外围电子构型为2s22p6的原子为Ne元素、③2p轨道为半满的元素为N元素、④电负性最大的元素是F元素,所以Na元素和F元素、N元素之间易形成离子键,易形成离子化合物,
故选A.
点评 本题考查离子化合物和化学键的关系,为高频考点,侧重考查基本概念,明确概念内涵是解本题关键,注意不能根据是否含有金属元素判断离子化合物,如氯化铝是共价化合物,为易错点.


科目:高中化学 来源: 题型:解答题
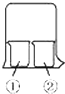 使用如图所示装置进行化学小实验,请填写下列空白:
使用如图所示装置进行化学小实验,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q | B. | 平衡时甲中C的体积分数比乙中小 | ||
| C. | 达到平衡时,甲中A的转化率为90% | D. | Q1+Q2>Q |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
| C | 石棉绒与过氧化钠 | 与CO2和水气反应,产生O2 |
| D | NaOH | 吸收未反应的CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com