
| 2.0×10-12 |
| 1×10-9 |
| 2.0×10-12 |
| 10-7 |
| 2.0×10-12 |
| 10-7 |
| 2.0×10-12 |
| 1×10-9 |
| 2×10-3y-1×10-4x |
| x+y |


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 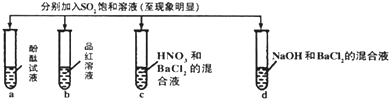 | ||||
| 记录 | 选项 | 试管a中 | 试管b中 | 试管c中 | 试管d中 |
| A | 无色 | 无色 | 无现象 | 无色溶液 | |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 无色 | 无色 | 白色沉淀 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2溶液 |
| B、饱和Na2CO3溶液 |
| C、Ca(ClO)2溶液 |
| D、Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素原子 | 性质和结构特点 |
| A | 原子中没有成对电子 |
| B | 基态原子中成对的电子的对数与单个电子的数目相同 |
| C | 基态原子的价电子排布式为(n+1)sn(n+1)pn+1 |
| D | C、D位于同周期的相邻元素,电负性:D大于C |
| E | E处于元素周期表的第8列 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com