
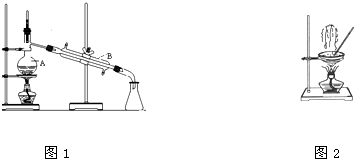
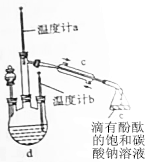
 ��1����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
��1����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺���� ��1������������״ȷ���������ƣ���ʯ�����Ƭ�ɷ����У�
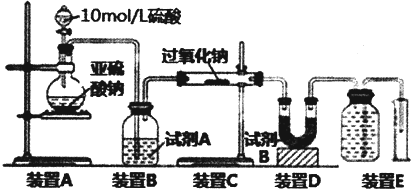
��2�����ε��ᴿ�У�Ϊ�˱�֤����������ȫ��ȥ��ÿһ�������Լ�������������NaOH��Һ��Ŀ���dz�ȥþ���ӣ���BaCl2��Һ��Ŀ���dz�ȥ��������ӣ���Na2CO3��Һ��Ŀ���dz�ȥ�����Ӻ����ı����ӣ��ɴ˿�֪��Na2CO3��Һ�ļ���һ����BaCl2��Һ֮��Ϊ�˲�ʹ�����ij����ܽ⣬һ��Ҫ�ڹ��˺��ټ����ᣬ�ݴ�ȷ�����Լ���˳��
��� �⣺��1��AΪ������ƿ��BΪ�����ܣ���ʯ�����Ƭ�ɷ�ֹ���У�װ��ͼ2��ʢ��Һ�����������������ʴ�Ϊ��������ƿ�������ܣ���ֹ���У�������
��2�����ε��ᴿ�У�Ϊ�˱�֤����������ȫ��ȥ��ÿһ�������Լ�������������NaOH��Һ��Ŀ���dz�ȥþ���ӣ���BaCl2��Һ��Ŀ���dz�ȥ��������ӣ���Na2CO3��Һ��Ŀ���dz�ȥ�����Ӻ����ı����ӣ��ɴ˿�֪��Na2CO3��Һ�ļ���һ����BaCl2��Һ֮����һ���ڢ�֮��Ϊ�˲�ʹ�����ij����ܽ⣬һ��Ҫ�ڹ��˺��ټ����ᣬ�����ڢ�֮�ʲ���˳������Ǣڢۢ٢ݢܻ�ۢڢ٢ݢܻ�ۢ٢ڢݢܣ��ʴ�Ϊ���ڢۢ٢ݢܻ�ۢڢ٢ݢܻ�ۢ٢ڢݢܣ�
���� ���⿼�鳣��������ʹ�úͻ�ѧ���������ķ����Լ����ε��ᴿ����Ŀ�ѶȲ���ע����ѧϰ�м�ǿ����֪ʶ�Ļ��ۣ�


 ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ890.3 kJmor-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4��g��+202 ��g���TC02 ��g��+2H20��g����H=-890.3kJ mol-1 | |
| B�� | 500 V��30MPa�£���0.5molN2��1.5 molH2�����ܱյ������г�ַ�Ӧ���� NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ N2��g��+3H2 ��g��$?_{500�桢30Mp}^{����}$2NH3��g����H=-38.6 kJmol-1 | |
| C�� | ͬ��ͬѹ�£������ʵ�����H2��������C12�ڹ��պ͵�ȼ�����³�ַ�Ӧ����������������ͬ | |
| D�� | ��֪�к���Ϊ57.3 kJ/mol����ϡ����������������Һ��Ӧ���Ȼ�ѧ����ʽΪ 2H+��aq��+SO42-��aq��+Ba2+��aq��+20H-��aq��=BaS04 ��s��+2H20��l����H=-57.3kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
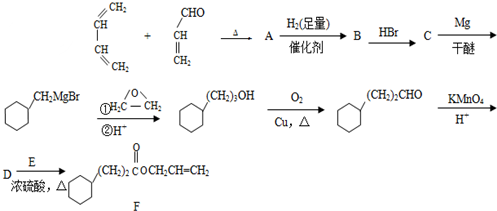

 ��A�����������ŵ�������ȩ����̼̼˫����
��A�����������ŵ�������ȩ����̼̼˫���� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ᶡ���е㡢�ܽ������±���
���ᶡ���е㡢�ܽ������±���| ���� | ���� | 1-���� | ���ᶡ�� | 90%Ũ���� |
| �е� | 117.9�� | 117.2�� | 126.3�� | 338.0�� |
| �ܽ��� | ����ˮ���л��ܼ� | ����ˮ���л��ܼ� | ����ˮ�������л��ܼ� | ��ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaNO2��������������Ӧ | B�� | ����1molN2ʱת�Ƶĵ�����Ϊ3mol | ||
| C�� | NH4Cl�е�NԪ�ر���ԭ | D�� | N2�������������»�ԭ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com