
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
分析 形成原电池时,活泼金属做负极,根据电极反应现象首先判断电池的正负极,再判断金属的活泼性强弱,电子从负极沿导线流向正极,据此分析解答.
解答 解:形成原电池时,活泼金属做负极,若a、b相连时,a为负极,则金属活动性a>b;c、d相连时,电流由d到c,所以d为正极,金属活泼性为:c>d;a、c相连时,c极上产生大量气泡,说明在c极上产生氢气,c极上发生还原反应,c极为正极,则活动性a>c;b、d相连时,d极板溶解,则金属活动性d>b,所以四种金属的活动性顺序为a>c>d>b,故选B.
点评 本题考查金属的活动性的顺序强弱比较,题目难度不大,本题考查角度为形成原电池反应,注意活泼金属做负极.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 生成1 mol N2,电子转移总数为3NA | B. | 生成1 mol N2,电子转移总数为5NA | ||
| C. | 溶解1 mol Zn,电子转移总数为2NA | D. | 溶解1 mol Zn,电子转移总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 | |
| B. | 滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 | |
| C. | 测得反应后溶液中Na+与Cl-的个数比为1:1 | |
| D. | 滴入几滴酚酞试液,酚酞试液不变色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
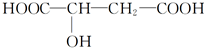 .苹果酸可能发生的反应是( )
.苹果酸可能发生的反应是( )| A. | 只有①②③ | B. | 只有②③④ | C. | 只有①②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
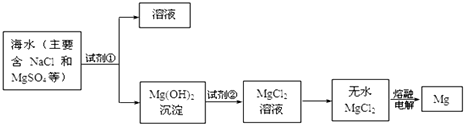
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | 将铝片改为铝粉,做铝与氧气反应的实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+
,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+ →
→ ,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图
,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图 ,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T
,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com