
在标准状况下将1.92 g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混合气体1.12 L,则反应消耗HNO3的物质的量为( )
A.0.8 mol B.0.6 mol
C.0.11 mol D.无法计算
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革的还原剂,它受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2 制得。实验室模拟该工业过程的装置如图所示。回答下列问题:
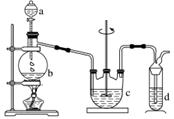
(1)b中反应的离子方程式为_______________________________________________________,
c中试剂为____________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是____________。
(3)d中的试剂为______________。
(4)实验中要控制SO2生成速率,可以采取的措施有
________________________________________________________________________
__________________________________________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入SO2不能过量,原因是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H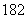 O与D
O与D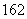 O的相对分子质量相同
O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.所有铵盐受热均可以分解,产物均有NH3
B.硝酸铵受热易分解爆炸,实验室常用加热氯化铵与氢氧化钙的固体混合物制备氨气
C.在盛有硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液的试管中,滴加少量NaOH溶液,在试管口用湿润的红色石蕊试纸检验,试纸变蓝
D.铵盐都易溶于水,其水溶液均呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室模拟合成氨和氨催化氧化的流程如下:


已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从图中选择制取气体的合适装置:氮气______________、氢气______________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有________、_________。
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,________(“会”或“不会”)发生倒吸,原因是______________________________________________________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是____________________________________________,
锥形瓶中还可观察到的现象是________________________________________________。
(5)写出乙装置中氨氧化的化学方程式:____________________________________
________________________________________________________________________。
(6)反应结束后锥形瓶内的溶液中含有的离子为H+、OH-、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去):
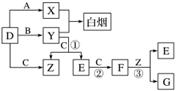
请回答下列问题:
(1)D的化学式为________。
(2)反应③的离子方程式为________________________________________。
(3)Y和E在一定条件下可反应生成B和Z,利用该反应可消除E对环境的污染,该反应的化学方程式为_________________________________________________________。
(4)0.1 mol·L-1的X溶液和0.1 mol·L-1的Y溶液等体积混合,溶液呈________性(填“酸”、“碱”或“中”),原因是________________(用离子方程式说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com