
| △ |
| m |
| M |
| △ |
| 98g |
| 98g/mol |
| 2g |
| 18g/mol |
| 1 |
| 9 |
| 1 |
| 9 |
| 1 |
| 9 |
| △ |
| 33 |
| 340 |
| 1 |
| 170 |
| 33 |
| 340 |


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
| A、①② | B、②③④⑤ |
| C、①②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgSO4溶液:c(Mg2+)+c(H+)=c (SO42-)+c(OH-) |
| B、将0.2mol?L-1CH3COOH溶液与0.1mo1?L-1NaOH溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C、将pH=2的盐酸与0.01 mo1?L-1氨水等体积混合:c(NH4+)=c (Cl-) |
| D、由AgCl和AgI固体混合物与水形成的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5% | B、7.5% |
| C、9.5% | D、10% |
查看答案和解析>>
科目:高中化学 来源: 题型:
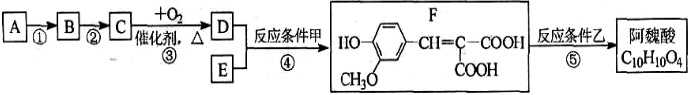
| 反应条件甲 |
| 反应条件乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
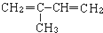 、⑤ClCH=CHCl、⑥
、⑤ClCH=CHCl、⑥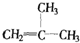 、⑦
、⑦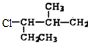 、⑧
、⑧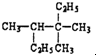 、⑨
、⑨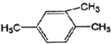
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关 |
| B、漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| C、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作消毒剂和净水剂 |
| D、在食品袋中放入盛有硅胶、生石灰的透气小袋,可防止食物受潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、久置的氯水与新制的氯水,都能使有色布条褪色 |
| B、氯气、液氯和氯水是同一种物质 |
| C、碘化钾溶液中加淀粉溶液变蓝色 |
| D、加碘盐就是在食盐中加入适量的碘酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:

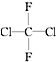 和
和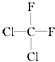
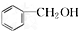 和
和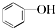
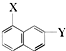 和
和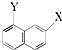
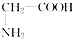
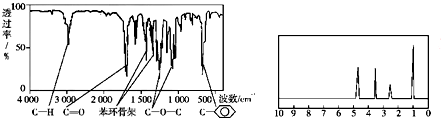
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com