
【题目】
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)G位于周期表的____区(填“s”、“ p”、“d ”或“ds”)。
(2)画出W基态原子的核外电子排布图_______。
(3)A2Y的VSEPR模型名称为______。
(4)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理.写出X2Y的电子式____,其中心原子的杂化软道类型是______,1个X2Y分子中含的π键数为______。
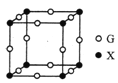
(5)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。
(6)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为______cm。
【答案】 ds ![]() (2) 四面体
(2) 四面体 ![]() sp 2 Cu3N
sp 2 Cu3N 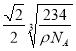
【解析】有A、X、Y、Z、W、M、G等原子序数依次增大的前四周期元素,A原子核外电子总数与其周期数相同,则A是H;X基态原子的L层中有3个未成对电子,所以X是N;Y基态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反,所以Y是O;Z原子核外p电子数比s电子数多l个,则Z是Na;W原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817,I3=2745 I4=11575,这说明最高价是+3价,则W是Al;M元素的主族数与周期数相差4,则M是Cl;G基态原子最外层电子数为1,其余各电子层均充满电子,因此G是Cu。
(1)铜位于周期表的ds区。(2)基态铝原子的核外电子数是13,则其核外电子排布图为![]() 。(3)H2O分子中O的价层电子对数=2+(6-2×1)/2=4,所以VSEPR模型名称为四面体。(4)已知为N2O分子中O原子只与一个N原子相连,与CO2互为等电子体,则其电子式为
。(3)H2O分子中O的价层电子对数=2+(6-2×1)/2=4,所以VSEPR模型名称为四面体。(4)已知为N2O分子中O原子只与一个N原子相连,与CO2互为等电子体,则其电子式为![]() ,CO2是直线形结构,其中心原子的杂化软道类型是sp。双键中含有一个π键,因此1个N2O分子中含的π键数为2;(5)根据晶胞结构可知N原子个数=8×1/8=1,Cu原子个数=12×1/4=3,因此其化学式为Cu3N。(6)氯化钠晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的钠离子中心间距离为面对角线的一半。晶胞中含有离子的个数均是4个,则晶胞边长是
,CO2是直线形结构,其中心原子的杂化软道类型是sp。双键中含有一个π键,因此1个N2O分子中含的π键数为2;(5)根据晶胞结构可知N原子个数=8×1/8=1,Cu原子个数=12×1/4=3,因此其化学式为Cu3N。(6)氯化钠晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的钠离子中心间距离为面对角线的一半。晶胞中含有离子的个数均是4个,则晶胞边长是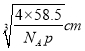 ,则晶体中两个距离最近的钠离子中心间距离为
,则晶体中两个距离最近的钠离子中心间距离为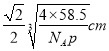 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区元素的是________(填元素符号)。
(2)⑥和⑦形成的分子中各个原子均满足8电子稳定结构,其立体构型为________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子和⑦形成的分子,中心原子上的价层电子对数为_______。
(4)元素⑦和⑧形成的化合物的电子式为__________。
(5)元素⑩的基态+2价离子的电子排布式是__________。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 金刚石和石墨是同种物质
B. C60和 CO2均是碳元素的化合物
C. 氧气和臭氧是氧元素的同素异形体
D. 农村常用草木灰和碳酸氢铵一起施用来增加肥效
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C===K2S+N2↑ +3CO2↑。该反应的还原剂是 ,氧化剂是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O==2Cu+2Li++2OH-,下列说法不正确的是

A. 放电时,正极的电极反应式为Cu2O+H2O+2e-=2OH-+2Cu
B. 放电时,电子透过固体电解质向Li极移动
C. 通空气时,铜电极被腐蚀,表面产生Cu2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求完成有关填空:
(1)A、B两种有机物分子式都是C9H11NO2。
化合物A是天然蛋白质的水解产物,光谱测定显示,分子结构中不存在甲基。则A的结构简式是____________________。
化合物B是某种分子式为C9H12的芳香烃的一硝化后的唯一产物(硝基连在苯环上)。则B的结构简式是____________________。
(2)烷基取代苯________________________________________________________________________________________________________________________________________________ ; __________________________________ ;__________________________________ ;___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联苯的结构简式如右图(![]() ),下列有关联苯的说法中正确的是( )
),下列有关联苯的说法中正确的是( )
A. 它和蒽(![]() )同属于芳香烃,两者互为同系物
)同属于芳香烃,两者互为同系物
B. 联苯的一氯代物有4种
C. 1mol联苯最多可以和6molH2发生加成反应
D. 它容易发生加成反应、取代反应,也容易被强氧化剂(如:酸性KMnO4溶液)氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B. 等质量的烃CxHy完全燃烧耗氧量的多少取决于y/x的值的大小,y/x的值越大,耗氧量越多
C. 某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4;若体积减少,则y<4;否则y>4
D. 质量相同的两种有机物完全且充分燃烧产生等量的二氧化碳,则这两种有机物中碳元素的质量分数一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次递增。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D四种元素第一电离能最大的是_______________。
(2)B的氯化物的熔点比D的氯化物的熔点__________(填“高”或“低”),理由是
__________________________________________________。
(3)E的低价氧化物分子的立体构型是_________________,用KMnO4酸性溶液吸收该氧化物时,MnO4-被还原为Mn2+,该反应的离子方程式为______________________________________。
(4)F的核外电子排布式是___________。
(5)A、F形成某种化合物的晶胞结构如下图所示(其中A显-3价),该化合物的化学式是_________________,若晶胞边长为a cm,阿伏伽德罗常数为NA,则该晶体的密度计算式为ρ=___________g/cm3(用含a、NA的符号表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com