
| A. | 锌锰干电池工作一段时间后碳棒变细 | |
| B. | 铅蓄电池工作一段时间后酸性会增强 | |
| C. | 水和水煤气都是一级能源 | |
| D. | 铁与H2SO4反应时,加入少量CuSO4溶液时,可使反应加速 |
分析 A.锌锰干电池中,正极上得电子发生还原反应;
B、根据电池反应Pb+PbO2+2H2SO4=2PbSO4+2H2O判断铅蓄电池的酸碱性变化;
C、水煤气是通过煤制取,成分是一氧化碳和氢气;
D、铁与H2SO4反应时,加入少量CuSO4溶液时,可以形成原电池.
解答 解:A.锌锰干电池中,负极上锌失电子发生氧化反应生成锌离子,所以锌逐渐被腐蚀而变细,正极上得电子发生还原反应,故A错误;
B、根据电池反应Pb+PbO2+2H2SO4=2PbSO4+2H2O知,放电过程中硫酸参加反应,所以随着反应的进行,氢离子浓度减小,所以溶液的酸性会减弱,故B错误;
C、水煤气是通过煤制取的,是二级能源,故C错误;
D、铁与H2SO4反应时,加入少量CuSO4溶液时,金属铁可以将铜置换出来,会形成原电池,加快反应速率,故D正确.
故选D.
点评 本题涉及原电池的工作原理以及应用、能源、影响化学反应速率的因素等知识,属于综合知识的考查,难度中等.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水或酸性高锰酸钾褪色均属于加成反应 | |
| B. | 用乙醇与浓硫酸加热至170℃制乙烯的反应属于取代反应 | |
| C. | 用“地沟油”生产生物柴油只发生酯化反应 | |
| D. | 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 | B. | AgNO3 | C. | Na2SO3 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| M | N | ||
| X | Y |
| A. | X位于三周期 IIA,其单质可采用电解熔融MgCl2制备 | |
| B. | 元素最高价氧化物的水化物中,酸性最强的是HNO3 | |
| C. | 气体分子(MN)2 的电子式为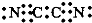 | |
| D. | (MN)2其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=2NaCN+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁中含有碳,抗腐蚀能力比纯铁弱 | |
| B. | 用锡焊接的铁质器件,焊接处易生锈 | |
| C. | 在铁制品上镀铜时,镀件(待镀金属)为阳极,铜盐为电镀液 | |
| D. | 铁制钥匙表面镀上一层锌,钥匙不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
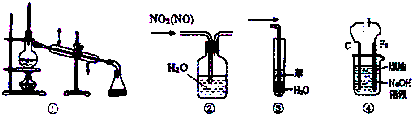
| A. | 装置①常用于互溶但沸点不同的液体混合物的分离 | |
| B. | 用装置②可除去NO2中的NO | |
| C. | 装置③可用于吸收NH3或HCl气体,并防止倒吸 | |
| D. | 装置④可用于制备Fe(0H)2并能 较长时间观察其颜色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com