
���淴Ӧ2SO2��g����O2��g��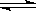 2SO3��g����������ʼ�����ﵽ��ƽ�⣬��ʱSO2��O2�����ʵ���֮��Ϊ2��1������ȡij�ִ�ʩ������SO2��O2��������һЩ�����ٴδﵽƽ�⣬����˵����ȷ���ǣ�
2SO3��g����������ʼ�����ﵽ��ƽ�⣬��ʱSO2��O2�����ʵ���֮��Ϊ2��1������ȡij�ִ�ʩ������SO2��O2��������һЩ�����ٴδﵽƽ�⣬����˵����ȷ���ǣ�
A����ƽ����ϵ�У�SO2��O2���ʵ���֮����Ϊ2��1
B��ƽ��������Ӧ�����ƶ���ԭ��������Ӧ���������淴Ӧ���ʼ�С
C����ƽ����ϵ���ƽ����ϵ�Ƚϣ�SO3��Ũ�ȿ϶�����
D��������ȡ�Ĵ�ʩ����С�������ݻ������¾�ƽ����SO2��O2��ת����֮�ȶ���1��1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�������Ҫ�ò����������в�����������ͬ����( )
�� ���� �� ���� �� �ܽ� �� ������ƿת��Һ��
A���ٺ͢� B���ٺ͢� C���ٺ͢� D���ۺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 25�桢101 kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8 kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
25�桢101 kPa�£�2g����ȼ������Һ̬ˮ���ų�285.8 kJ��������ʾ�÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A��2H2(g)+O2(g) == 2H2O(1) ��H�� -285.8 kJ��mol
B��2H2(g)+ O2(g) == 2H2O(1) ��H�� +571.6 kJ��mol
C��2H2(g)+O2(g) == 2H2O(g) ��H�� -571.6 kJ��mol
D��H2(g)+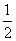 O2(g) == H2O(1) ��H�� -285.8 kJ��mol
O2(g) == H2O(1) ��H�� -285.8 kJ��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ����a��ʾ���ȷ�ӦX(g)��Y(g)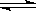 Z(g)��M(g)��N(s)���й�����X��ת������ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ��
Z(g)��M(g)��N(s)���й�����X��ת������ʱ��仯�Ĺ�ϵ����Ҫ�ı���ʼ������ʹ��Ӧ���̰�b���߽��У��ɲ�ȡ�Ĵ�ʩ��
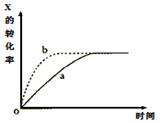
A����С��� B���Ӵ�X��Ͷ����
C����ѹ D�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�ܱ���ƿ�У���25��ʱ������ƽ�⣺2NO2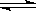 N2O4������Ӧ���ȣ�������ƿ����100���ˮ�У������м��������в���ı����
N2O4������Ӧ���ȣ�������ƿ����100���ˮ�У������м��������в���ı����
����ɫ ��ƽ�������� ������ ��ѹǿ ���ܶ�
A���ٺ͢� B���ں͢� C���ܺ͢� D���ۺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£�ij�ݻ��㶨���ܱ������з������¿��淴Ӧ
CO��g����H2O��g��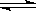 H2��g����CO2��g�� ��H��0
H2��g����CO2��g�� ��H��0
����Ӧ��ƽ��ʱ����������и����ʾ�Ϊnmol����ʹH2��ƽ��Ũ������һ������������������ʱ�����д�ʩ���Բ��õ���
A�������¶� B���ټ���2n mol H2
C���ټ���nmol CO��nmol H2O D���ټ���2n mol CO2��2n mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
H2S����ˮ�ĵ��뷽��ʽΪ ��
����H2S��Һ�м���Ũ����ʱ������ƽ���� �ƶ���c(H��) ��������С�����䣩��c(S2��) ��������С�����䣩��
����H2S��Һ�м���NaOH���壬����ƽ���� �ƶ���c(H��) ��������С�����䣩��c(S2��) ��������С�����䣩��
����ҪʹH2S��Һ��c(HS��)������ʹH2S�ĵ���ƽ�������ƶ������Լ��� ��
����H2S��Һ�м�ˮ��c(HS��) ��������С�����䣩����ҺpH ��������С�����䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݵ���������Ӧ���Ȼ�ѧ����ʽ
����I2(g) + H2(g) 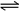 2 HI(g) ��H=��9.48 kJ/mol
2 HI(g) ��H=��9.48 kJ/mol
����I2(s) + H2(g) 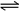 2 HI(g) ��H=��26.48 kJ/mol
2 HI(g) ��H=��26.48 kJ/mol
�����ж���ȷ����
A��254 g I2(g)��ͨ��2 g H2(g)����Ӧ����9.48 kJ
B��1 mol��̬����1 mol��̬���������������17.00 kJ
C����Ӧ���IJ���ȷ�Ӧ���IJ����ȶ�
D����Ӧ���ķ�Ӧ���������ȷ�Ӧ���ķ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��Ԫ��A�ǵ������ڢ�A��Ԫ�أ�AԪ���������ַǽ���Ԫ�ؿ�������ӻ�����ס�д���Ļ�ѧʽ________��
��2�������е���̬�⻯���У�Ԫ��B���⻯�����ȶ���д��Ԫ��B�����ڱ��е�λ��____________________ ��
��3������Ԫ��C�γɵ�ij���������Һ�����ڼ���CO2����Ԫ��C�ļ�������Ԫ��A�ļ����ӵİ뾶��С��ϵ��________ (�����ӷ��ű�ʾ)��Ԫ��D��ԭ��������Ԫ��CС8��д��Ԫ��D�ĵ�����CO2��ȼ�յĻ�ѧ����ʽ________ ��
��4��Ԫ��E�ǵ��������м����Ӱ뾶��С��Ԫ�أ�Ԫ��F�ǵ���������ԭ�Ӱ뾶����Ԫ�أ�д��Ԫ��E�ĵ�����Ԫ��F������������Ӧˮ���ﷴӦ�ĵ����ӷ���ʽ__________________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com