
已知X、Y、Z、W是原子序数依次增大的短周期元素,这些元素的其他信息如下表。下列说法正确的是
元素 | 信息 |
X | K层电子数是L层电子数的2倍 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | 所处的周期序数与族序数相等 |
W | 最高价氧化物对应的水化物酸性最强 |
A.W的阴离子半径大于Z的阳离子半径
B.Y的氢化物比W的氢化物稳定
C.Z的最高价氧化物对应的水化物不能够溶于Y的最高价氧化物对应的水化物
D.X在氧气中加热反应生成X2O2
AC
【解析】
试题分析:K层电子数是L层电子数的2倍,则L层电子数是1个,因此X的原子序数是3,是锂元素;一种核素在考古时常用来鉴定一些文物的年代,则Y是碳元素;所处的周期序数与族序数相等,奇热Z的原子序数大于碳元素,所以Z只能是第三周期第ⅢA元素,是铝元素;最高价氧化物对应的水化物酸性最强,因此W是氯元素,则氯离子有3个电子层,铝离子有2个电子层,所以W的阴离子半径大于Z的阳离子半径,A正确;B、非金属性越强氢化物的稳定性越强,非金属性是Cl大于C,因此W的氢化物比Y的氢化物稳定,B不正确;C、氢氧化铝是两性氢氧化物但不能溶于弱酸碳酸中,C正确;D、金属锂在氧气中燃烧只能生成Li2O,D不正确,答案选AC。
考点:考查元素周期表的结构以及元素周期律的应用


科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷乙(解析版) 题型:选择题
在100mL含等物质的量的HBr和H2SO3的溶液里通入0.01mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。原溶液中HBr和H2SO3的浓度都等于:
A.0.0075mol·L-1 B.0.008mol·L-1 C.0.075mol·L-1 D.0.08mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省江门市高二调研测试理综化学试卷(解析版) 题型:选择题
常温下,在0.1mol/L的碳酸钠溶液中,下列离子浓度的关系式正确的是
A.2c(H2CO3)+c(HCO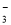 )+c(H+) = c(OH-)
)+c(H+) = c(OH-)
B.c(Na+) = c(HCO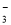 )+c(H2CO3)+ 2c(CO
)+c(H2CO3)+ 2c(CO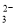 )
)
C.c(Na+)>c(H+)>c(OH-)>c(CO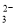 )
)
D.c(Na+)+c(H+) = c(HCO )+c(OH-)+ 2c(CO
)+c(OH-)+ 2c(CO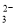 )
)
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
下列物质中都是既含有离子键又含有共价键的一组是( )
A、NaOH, H2O, NH4Cl
B、KOH, Na2O2, (NH4)2S
C、MgO,CaBr2, NaCl
D、Na2SO4, HCl, MgCl2
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:实验题
(17分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:

称取研细的黄铜矿样品1.150g,在空气存在的条件下进行煅烧。实验后取d中溶液的1/10置于锥形瓶中,用0.05mo1/L标准碘溶液进行滴定,初读数为0.10mL,终读数如右上图所示。
(1)黄铜矿煅烧的反应为8CuFeS2+21O2高温8Cu+4FeO+2Fe2O3+16SO2,该反应中被还原的元素是___(填元素符号)。
(2)标准碘溶液应盛放在(填“碱式”或“酸式”)________滴定管中;装液之前,滴定管要用标准碘溶液润洗2—3次,润洗的操作是: 。请用化学方程式表示滴定的原理: 。
(3)滴定终点的读数为 mL;通过计算可知,该黄铜矿的纯度为 。
(4)若去掉c装置,会使测定结果 (填“偏低”“偏高”或“无影响”)。
(5)假设实验操作均正确,测得黄铜矿的纯度偏低,可能的原因主要有 。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省揭阳市高三4月第二次模拟理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列叙述正确的是
A.Na2O和Na2O2的混合物共1mol,阴离子数目为NA
B.过量的Fe与Cl2反应生成0.1mol产物时失去的电子数为0.2NA
C.标准状况下,11.2 LCHCl3中含有C-Cl键的数目为1.5NA
D.一定条件下,2 mol H2和0.5 mol N2充分反应后可得到NH3分子数为NA
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列各组物质在不同条件下反应时,均能得到不同产物,其中主要是由于反应物的浓度不同而引起的是
A. Fe+H2SO4 B.Cu+HNO3 C. NaOH+ CO2 D. AlCl3 +NaOH
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%,下列反应类型能体现“绿色化学工艺”的是
A.化合反应 B.复分解反应 C.分解反应 D.取代反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省广州市越秀区高二下学期期末水平调研化学试卷(解析版) 题型:实验题
过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:CO(NH2)2+H2O2 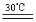 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
CO(NH2)2?H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如下:

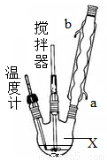
请回答下列问题:
(1)仪器X的名称是 ;冷凝管中冷却水从 (填“a”或“b”)口进入;
(2)反应器的加热方式是 。
(3)搅拌器是否可用铁质材料 (填“是”或“否”),原因是 ;
(4)步骤①采用减压蒸发的原因是 。
(5)母液可以循环使用提高原料利用率,若欲从母液中分离出H2O2和尿素, 可采用的操作是
A.盐析、过滤 B.减压蒸馏、结晶
C.分液、过滤 D.常压蒸馏、萃取
(6)准确称取0.5000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL6mol·L-1H2SO4,用0.1000mol?L-1KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2?H2O2的质量分数为 ;若滴定前滴定管尖嘴处有气泡,滴定后消失,则测得的过氧化尿素含量 (填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com