
����Ŀ���������Ʊ���Ϊ��ҵ�Σ���Ư�ס���Ƶȷ���Ӧ�ù㷺����ľ̿��Ũ���ᡢˮ��ͭΪԭ�����ɵ�һ��������������Ʒ�Ӧ�Ʊ��������Ƶ�װ������ͼ��ʾ(���ּг�װ����)��

��֪�������£���2NO+Na2O2��2NaNO2
�����������£�NO ��![]() ������
������![]() ��Ӧ����
��Ӧ����![]() �� Mn2+
�� Mn2+
��B �е� Cu ����
���������գ�
(1)д��Ũ������ľ̿��Ӧ�Ļ�ѧ����ʽ__________��
(2)������װ�õ������ԣ�װ��ҩƷ������е�һ��������______________��
(3)D װ�õ������� ________��
(4)������ C �����г�������������и�����̼���ƺ�_______��Ϊ���������Щ������Ӧ�� B��Cװ�ü�����װ�� E��E ��ʢ�ŵ�ҩƷ����________��
(5)�� 7.8g ����������ȫת����Ϊ�������ƣ�������������Ҫľ̿_______________g��
���𰸡�C + 4HNO3(Ũ) ![]() CO2 + 4NO2��+ 2H2O �ų�װ���ڵĿ��� ����β������ֹ��Ⱦ���� NaOH ��ʯ�� 1.2
CO2 + 4NO2��+ 2H2O �ų�װ���ڵĿ��� ����β������ֹ��Ⱦ���� NaOH ��ʯ�� 1.2
��������
ľ̿��Ũ���ᷴӦ���ɶ�����̼������������ˮ��������������ˮ����һ�������������ͭ��Ӧ����һ������������ͭ��ˮ��NO�������Ʒ�Ӧ�����������ƣ�NO�ױ��������������װ�����ų����������������к���ˮ�����Ͷ�����̼��Ϊ�˼���������������ɣ�Ҫ�����徻�����ӡ�
(1)Ũ������ľ̿��Ӧ���ɶ�����̼������������ˮ���仯ѧ����ʽC + 4HNO3(Ũ)![]() CO2��+ 4NO2��+ 2H2O���ʴ�Ϊ��C + 4HNO3(Ũ)
CO2��+ 4NO2��+ 2H2O���ʴ�Ϊ��C + 4HNO3(Ũ) ![]() CO2+ 4NO2��+ 2H2O��
CO2+ 4NO2��+ 2H2O��
(2)������װ�õ������ԣ�װ��ҩƷ��NO�ױ���������˱�����е�һ���������ų�װ���ڵĿ������ų�װ���ڵĿ�����
(3)NO����Ⱦ���������D װ�õ������Ǵ���β������ֹ��Ⱦ�������ʴ�Ϊ������β������ֹ��Ⱦ������
(4)��B�г�����������Ҫ��NO������CO2��H2O����Щ���嶼Ҫ��������Ʒ�Ӧ����˾����� C �����г�������������и�����̼���ƺ�NaOH��Ϊ���������Щ������Ӧ�� B��Cװ�ü�����װ��E��E�����ü�Ҫ����CO2����Ҫ����H2O�����E��ʢ�ŵ�ҩƷ���Ƽ�ʯ�ң��ʴ�Ϊ��NaOH����ʯ�ҡ�
(5) n��Na2O2��=0.1mol������C + 4HNO3(Ũ) ![]() CO2+ 4NO2��+ 2H2O��3NO2+H2O=2HNO3+NO��3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O��2NO+Na2O2=2NaNO2��Ӧ��ϵ��֪��C--Na2O2,��������C������=12g/mol��0.1mol=1.2g��
CO2+ 4NO2��+ 2H2O��3NO2+H2O=2HNO3+NO��3Cu+8HNO3=3Cu��NO3��2+2NO��+4H2O��2NO+Na2O2=2NaNO2��Ӧ��ϵ��֪��C--Na2O2,��������C������=12g/mol��0.1mol=1.2g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С������ʵ���ʾ��ͼ��ͼ��ʾ��ͼ�С�������ʾ�������� M��һ�ִ�������������壬YΪ��һ�����壬E���к���ɫ���������ʵ����������ֻ��������������ѡȡ��Na2CO3��Na2O2��NaCl��Na2O��CaCl2��(NH4)2CO3����ʯ�ҵȹ��弰����ˮ���ݴ�ʵ�飬���������գ�
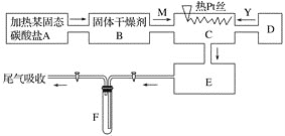
(1)A������װ�õ���Ҫ������ҩƷ��______________________��
(2)B����ѡ�ĸ������________����������______________________________��
(3)C�з�������Ҫ��Ӧ�Ļ�ѧ����ʽ��________________________________��
(4)��ȡY�����Dװ�����õ���Ҫ������__________________________��
��ȡY����Ļ�ѧ����ʽ��________________________��
(5)F�з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.0mol/L��NaOH��Һ�к�ijŨ�ȵ�H2SO4��Һ����ˮ��Һ��pH������NaOH��Һ������仯��ϵ��ͼ��ʾ����ԭH2SO4��Һ�����ʵ���Ũ�Ⱥ���ȫ��Ӧ����Һ�Ĵ�������ǣ� ��

A��1.0 mol/L��20 mL B��0.5 mol/L��40 mL
C��0.5 mol/L��80 mL D��1.0 mol/L��80 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���ô�CuO��ĩ������Fe2O3��FeO���ʣ��Ʊ�������CuCl2��xH2O���塣
�йؽ������ӿ�ʼ�����ͳ�����ȫʱ��Һ��pH
���� | Cu2+ | Fe2+ | Fe3+ |
��ʼ����pH | 5.4 | 8.1 | 2.7 |
������ȫpH | 6.9 | 9.6 | 3.7 |
�Ʊ��������£�

(1)�����Լ�X��Ŀ���ǽ�Fe2+����ΪFe3+���Լ�X��_______��
(2)�����Լ�Y��Ŀ���ǵ�����Һ��pH���Լ�Y��______������pH�ķ�Χ��_____�����ɵĹ���Z��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҽ���䷽����϶��¹ڷ��ײ������ƾ������õ�Ч�������е�һζ��ҩ���˵���Ч�ɷֽṹ��ʽ��ͼ��ʾ������˵���������

A.�������Ƿ��㻯������������ֹ�����B.�����տɷ���ȡ�����ӳɡ���������ԭ��Ӧ
C.1mol ������������� 3molNaOHD.1 mol ����������� 7mol H2 ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Һ������Ũ�ȵ�˵������ȷ����
A.0.1mol��L-1NaHCO3��Һ��c(Na+)>c(CO32-)>c(H2CO3)>c(OH-)>c(H+)
B.Na2Sϡ��Һ��c(H+)=c(OH-)-2c(H2S)-c(HS-)
C.pH=1��NaHSO4��Һ��c(H+)=c(SO42-)+c(OH-)
D.�������ʵ�����NaHC2O4��Na2C2O4����Һ��2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����(N2H4)�Ƕ�Ԫ�����ˮ�еĵ��뷽��ʽ�백���ƣ�������һ�����뷴Ӧ��ƽ�ⳣ��ֵΪ____����֪��N2H4+H+![]() N2H5+��K=8.7��107��Kw=1��10-14���������������γɵ���ʽ�εĻ�ѧʽΪ____��
N2H5+��K=8.7��107��Kw=1��10-14���������������γɵ���ʽ�εĻ�ѧʽΪ____��
(2)������(H3PO2)��һԪ��ǿ�ᣬд������뷽��ʽ��_______��NaH2PO2��Һ��_______��������ԡ��������ԡ��������ԡ�����
(3)��֪Ksp(AgCl)=1.8��10-10������50mL0.018mol��L-1��AgNO3��Һ�м���50mL0.020mol��L-1�����ᣬ��Ϻ���Һ�е�Ag+��Ũ��Ϊ_______mol��L-1��
(4)��ͼ��ʾΪ��Ԫ��H2A��Һ�и��������ʵ�������(��)����ҺpH�ı仯����(25C)��

H2A�ĵ���ƽ�ⳣ��Ka1=_______����ҺpH=7ʱ�� =______��
=______��
(5)25��ʱ��amolL-1��ˮ��0.01molL-1������������ϣ�����Ϻ�������Һ��c(NH4+)=c(Cl-)���ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ���ƽ�ⳣ��Kb=_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ����һ��ǰ�����������͵�أ��������ܶ���Ŀǰ﮵�ص�ʮ�������Ҳ�����Ϊ���ȶ���ɰ�ȫ���ա���ͼ�Ƿ����ӵ�ع���ʾ��ͼ�����г��ʱF-���ҵ缫����缫�����й��ڸõ�ص�˵����ȷ���ǣ� ��

A.�ŵ�ʱ���缫�ĵ缫��ӦʽΪBi��3e-��3F-=BiF3
B.�ŵ�ʱ���ҵ缫���Ʊȼ缫��
C.���ʱ��������ÿͨ��1mole-���缫��������19g
D.���ʱ����ӵ�Դ���������ҵ缫����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ������������·�Ӧ��L(s)��aG(g) ![]() bR(g)���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ������ѹǿp1��p2���ɴ˿��ж�(����)
bR(g)���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ������ѹǿp1��p2���ɴ˿��ж�(����)
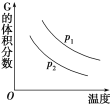
A.����ӦΪ���ȷ�Ӧ
B.G��ת�������¶����߶���С
C.��ѧ����ʽ�еļ�����a��b
D.����ѹǿ��������������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com