
| A. | CH3Br | B. | 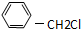 | C. | 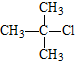 | D. | 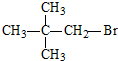 |
科目:高中化学 来源: 题型:选择题
 已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )| A. | 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水小 | |
| C. | 在pH=3的溶液中存在$\frac{c({R}^{2-})×c({H}_{2}R)}{c(H{R}^{-})}$=10-3 | |
| D. | 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体和溶液的本质区别是分散质粒子直径的大小 | |
| B. | 电解质与非电解质的本质区别,是在水溶液或熔融状态下中能否电离 | |
| C. | 科学家波尔首先提出原子核外的电子是在一定轨道上运动 | |
| D. | 具有相同质子数的微粒,一定属于同一种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-或HCO3-中的一种或两种 | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,可能有Ba2+ | |
| D. | 加入硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水冲洗,再涂上硼酸溶液 | |
| B. | 用稀硫酸溶液中和,再用水冲洗 | |
| C. | 用布擦去NaOH后,用稀硫酸溶液冲洗 | |
| D. | 用布擦去硫酸后,用大量水冲洗,再用3%-5%的碳酸氢钠溶液冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中只能含离子键 | B. | 共价化合物中可能含离子键 | ||
| C. | 共价键只存在于共价化合物中 | D. | 离子键只存在于离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和晶体硫熔融 | B. | 石墨和食盐熔化 | ||
| C. | 晶体碘和干冰的升华 | D. | 金属钠和硝酸钠的熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |
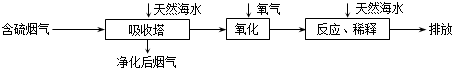
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com