
| A. | 中和反应是吸热反应 | |
| B. | 需要加热的反应都是吸热反应 | |
| C. | 断裂化学键要吸收能量 | |
| D. | 反应物总能量一定等于生成物总能量 |
分析 A、中和反应是酸和碱发生的反应,是放热反应;
B、有的放热反应需要高温条件发生;
C、断裂化学键需要吸收能量;
D、化学反应过程中一定伴随能量的变化,反应物总能量与生成物总能量一定不相等.
解答 解:A、中和反应是酸和碱发生的反应,是放热反应,故A错误;
B、有的放热反应需要高温条件发生,如铝热反应是放热反应,但需要加热,故B错误;
C、断裂化学键需要吸收能量,故C正确;
D、化学反应过程中一定伴随能量的变化,反应物总能量与生成物总能量一定不相等,故D错误;
故选C.
点评 本题考查了反应热效应的分析判断,中和热概念的应用,化学反应一定伴随能量变化,化学键的断裂过程是吸热过程,概念理解是解题关键.


科目:高中化学 来源: 题型:多选题
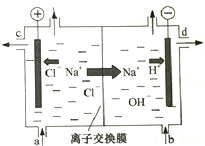 如图是离子交换膜法电解食盐水的示意图,离子交换膜只允许阳离子通过,上述精盐水需耍进行二次精制后才能作为离子交换膜电解槽的原料.对盐水进行二次精制的目的是 ( )(选填编号)
如图是离子交换膜法电解食盐水的示意图,离子交换膜只允许阳离子通过,上述精盐水需耍进行二次精制后才能作为离子交换膜电解槽的原料.对盐水进行二次精制的目的是 ( )(选填编号)| A. | 进一步降低Ca2+,Mg2+的浓度,提高烧碱纯度 | |
| B. | 进一步降低SO42-的浓度,提高烧碱纯度 | |
| C. | 防止杂质离子与碱生成的沉淀堵塞离子交换膜 | |
| D. | 防止溶液酸性或碱性过强,腐蚀离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的同系物分子中的碳原子数比苯分子中的碳原子数多 | |
| B. | 苯环受侧链影响易被氧化 | |
| C. | 侧链受苯环影响易被氧化 | |
| D. | 由于苯环和侧链的相互影响均易被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
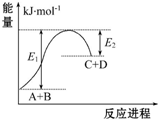
| A. | 该反应为放热反应 | |
| B. | 该反应吸收的能量为(E1-E2) | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应只有在加热条件下才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:K>Na>Li | B. | 热稳定性:HI>HCl>HF | ||
| C. | 非金属性:F>O>N | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某实验小组对一含有Al3+的未知溶液进行了如下分析:
某实验小组对一含有Al3+的未知溶液进行了如下分析:| A. | 该未知溶液中一定含有Al3+ Mg2+ H+三种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5 mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g | |
| D. | 若另一种离子为二价阳离子,则a=10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com