
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_____________________.
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式
正极反应_______________________________________________________,
负极反应_____________________________________________________________.
(3)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显.请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀
有关反应的化学方程式____________________.
劣质不锈钢腐蚀的实验现象___________________________________________.
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
LiSOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4SOCl2。
电池的总反应可表示为4Li+2SOCl2===4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为________________________。
(2)电池正极发生的电极反应为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都 正
确的是 ( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成反应、取代反应、消去反应 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
| C | 氧化反应、取代反应、消去反应 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、
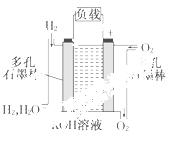
无噪音、高效率的特点.右图为氢氧燃料电池的结构示意图,电解质溶液为
KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、
负两极通入燃料电池时,便可在闭合回路中不断地产生电流。
试回答下列问题:
(1)图中通过负载的 电子流动方向________(填“向左”或“向右”).
电子流动方向________(填“向左”或“向右”).
(2)写出氢氧燃料电池工作时电极反应方程式和总反应方程式.
正极:________________________________________________________,
负极:________________________________________________________________,
总反应:__________________________________________________________.
(3 )为了获得氢气,除了充分利用太阳能外,工业上利用石油产品与水在催化剂作用下制取氢气.写出C3H8和H2O反应生成H2和CO的化学方程式:_____________________________________;
)为了获得氢气,除了充分利用太阳能外,工业上利用石油产品与水在催化剂作用下制取氢气.写出C3H8和H2O反应生成H2和CO的化学方程式:_____________________________________;
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,正极反应式为________________;
负极反应式为____________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 物质 组别 | 甲 | 乙 | 丙 |
| A | Al | HCl | NaOH |
| B | NH3 | O2 | HNO3 |
| C | SiO2 | NaOH | HF |
| D | SO2 | Ca(OH)2 | NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
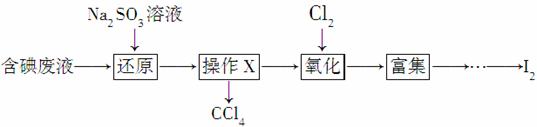
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为__________________;该操作将I2还原为I-的目的是________。
(2)操作X的名称为________。
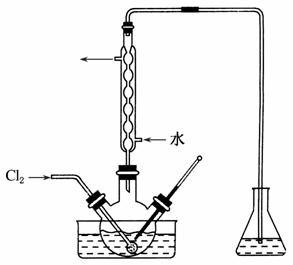
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40 ℃左右反应(实验装置如右图所示)。
实验控制在较低温度下进行的原因是__________;锥形瓶里盛放的溶液为__________。
(4)已知:5SO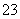 +2IO
+2IO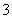 +2H+===I2+5SO
+2H+===I2+5SO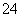 +H2O
+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO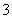 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO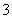 的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在________________________。
的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在________________________。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质
为淡黄色固体。下列推断中正确的是
A.原子半径由小到大的顺序:r(C)<r(D)<r(E)
B.元素D、E分别与A形成的化合物的热稳定性:E>D
C.元素D的最高价氧化物对应水化物的酸性比E的强
D.元素B分别与A、C形成的化合物中化学键的类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
甲在常温时为离子晶体,由X、Y两种元素组成,在甲中Xm+和Yn-的电子结构相同,甲、乙、丙、丁、
戊之间有如下反应关系
①甲+H2O H2↑+乙+丙↑
H2↑+乙+丙↑
②H2+丙—→丁气体
③乙+丙—→甲+戊+H2O
④戊+丁—→甲+己酸性
甲、戊、己依次是
A.NaCl、NaClO、HClO B .Na2S、Na2SO3、H2SO3
.Na2S、Na2SO3、H2SO3
C.CaCl2、CaClO2、HClO D.K2S、K2SO3、H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com