
【题目】相同条件下,下列各组热化学方程式中,△H2>△H1的是( )
A.2H2 (g)+O2(g)═2H2O(g)△H1; 2H2(g)+O2(g)═2H2O(l)△H2
B.S(g)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(g)△H2
C.CO(g)+ ![]() ?O2(g)═CO2(g)△H1; 2CO(g)+O2(g)═2CO2(g)△H2
?O2(g)═CO2(g)△H1; 2CO(g)+O2(g)═2CO2(g)△H2
D.![]() ?H2(g)+
?H2(g)+ ![]() ?Cl2(g)═HCl(g)△H1;H2(g)+Cl2(g)═2HCl(g)△H2
?Cl2(g)═HCl(g)△H1;H2(g)+Cl2(g)═2HCl(g)△H2
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】下列表格中各项分类都正确的一组是
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 生理盐水 | 苏打 | 液态KNO3 | 蔗糖 |
B | 熟石灰 | 海水 | 铜 | 乙醇 |
C | 胆矾 | 空气 | AgCl | CO2 |
D | 碱石灰 | 铝合金 | Na2SO4溶液 | 食醋 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。能判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。能判断该分解反应已经达到化学平衡的是
A. v(NH3)=2v(CO2)
B. 密闭容器中NH3体积分数不变
C. 密闭容器中混合气体的平均相对分子质量不变
D. 密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列有关化学基本概念的依据正确的是
A.纯净物与混合物:是否仅含有一种元素
B.酸:在水溶液里电离出的阳离子全部为H+的化合物
C.电解质与非电解质:辨别依据是水溶液是否导电
D.溶液与胶体:本质区别是能否发生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值,下列说法不正确的是
A. 将1mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA
B. 标准状况下,1L0.5molL-1乙酸溶液中含有氢离子总数为0.5NA
C. 3lg白磷分子含有共价键总数为1.5NA 已知:白磷(P4)为正四面体结构
D. 53克Na2CO3固体中含有CO32-总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制500mL浓度为2mol/L的NaOH溶液.选用容量瓶的规格和所需NaOH的质量分别为( )
A.100 mL 容量瓶、40 g
B.500 mL 容量瓶、40 g
C.100 mL 容量瓶、80 g
D.500 mL 容量瓶、80 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确的是
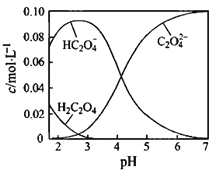
A. pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-)
B. c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+ c(C2O42-)
C. c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC2O4-)
D. pH=7的溶液中:c(Na+)=2c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于H2在O2中燃烧反应的描述,正确的是( )
A.该反应属于放热反应
B.断开H﹣H键放出能量
C.形成O﹣H键吸收能量
D.反应后生成物总能量升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com