
| A. | 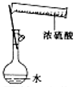 配制一定物质的量浓度的稀硫酸 | B. | 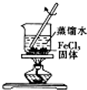 制取少量的Fe(OH)3胶体 | ||
| C. | 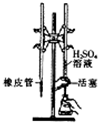 用H2SO4标准溶液滴定NaOH溶液 | D. | 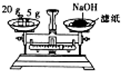 称量NaOH固体 |
分析 A.不能在容量瓶中稀释;
B.氯化铁饱和溶液水解制备胶体;
C.由图可知,酸式滴定管中为酸,滴定锥形瓶中NaOH溶液;
D.NaOH应在小烧杯中称量,且放在左盘.
解答 解:A.不能在容量瓶中稀释,应在烧杯中稀释、冷却后转移到容量瓶中,故A错误;
B.氯化铁饱和溶液水解制备胶体,图中为固体的溶解,故B错误;
C.由图可知,酸式滴定管中为酸,滴定锥形瓶中NaOH溶液,图中滴定操作合理,故C正确;
D.NaOH应在小烧杯中称量,且放在左盘,则图中称量操作不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制、胶体制备、中和滴定、实验基本操作及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 金属单质置换金属单质 | B. | 金属单质置换非金属单质 | ||
| C. | 非金属单质置换金属单质 | D. | 非金属单质置换非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃棒 | B. | 胶头滴管 | C. | 托盘天平 | D. | 容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇[CH3OH] | B. | 氯化钙[CaCl2] | C. | 尿素[CO(NH2)2] | D. | 亚硝酸钠[NaNO2] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图
原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图| A. | 将电能转化为化学能的装置 | B. | 电子由铜片经导线流向锌片 | ||
| C. | 锌片为负极,发生氧化反应 | D. | 铜片上发生的反应为Cu2++2e-═Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
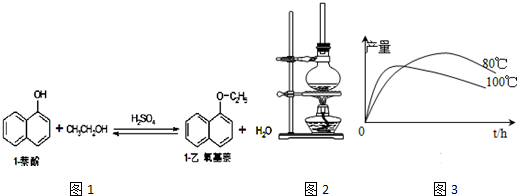
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com