
| A、水 |
| B、Na2CO3溶液 |
| C、溴水 |
| D、新制Cu(OH)2悬浊液 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、1mol?L-1的NaCl溶液表示1 L水中溶解有1 mol NaCl |
| B、容量瓶在使用前必须洁净、干燥 |
| C、需要950 mL 0.1mol?L-1的NaOH溶液,可以用500 mL、200 mL、250 mL的容量瓶各一只来配 |
| D、配制溶液定容时,不小心多加了一滴水,只能宣布配制失败,应重新配制 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶事先没有烘干 |
| B、定容时观察液面俯视 |
| C、定容时观察液面仰视 |
| D、转移液体至容量瓶时有少量液体流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+是该反应的催化剂 |
| B、反应速率与c(H2O2)无关 |
| C、H2O是该反应的催化剂 |
| D、v(IO3-)=v(HSO3-)=v(HSO4-)=v(I-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | Mn | Fe | |
| 电离能 kJ?mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
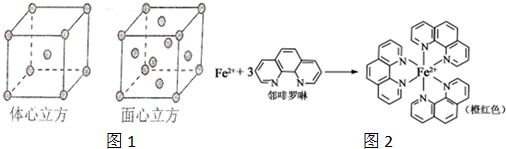
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、CaCO3与稀HCl反应制备CO2:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、向Ba(OH)2溶液中滴加KHSO4溶液至中性:Ba2++2OH-+2HSO4-═2H2O+BaSO4↓ |
| D、过量铁粉与氯化铁溶液反应:Fe3++Fe═2Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com