
�ڸ��¸�ѹ��CO���м��ߵĻ�ѧ���ԣ�������ֵ��ʻ��ﷴӦ��
��1�����ں��º��ݵ������ڽ��з�ӦC(s)+H2O(g)  CO(g)+H2(g)����������жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�� ��(����ĸ)
CO(g)+H2(g)����������жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�� ��(����ĸ)
a�������ڵ�ѹǿ���ֲ��� b��������H2Ũ����COŨ�����
c�������л��������ܶȱ��ֲ��� d��CO������������H2�������������
��2��COһ����ȼ�ϵ����ʹ�õĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2���õ�ظ����ĵ缫��ӦʽΪ ��
��3��һ�������£�CO��H2�ɺϳɼ��飬��Ӧ����ʽΪ��CO(g)+3H2(g)  CH4(g)+ H2O (g)
CH4(g)+ H2O (g)
��һ�������£��÷�Ӧ�ܹ��Է����е�ԭ���� ��
����֪H2(g)��CO(g)�� CH4(g)��ȼ���ȷֱ�Ϊ285��8 kJ��mol-1��283��0 kJ��mol-1��890,0 kJ��mol-1��
д��CO��H2��Ӧ����CH4��CO2���Ȼ�ѧ����ʽ�� ��
��4����ҵ�Ͽ�ͨ���״��ʻ�������ȡ�����������Ӧ����ʽΪ�� ��
CH3OH(g)+CO(g)  HCOOCH3(g) ��H=��29.1 kJ��mol-1
HCOOCH3(g) ��H=��29.1 kJ��mol-1
������Ա�Ը÷�Ӧ�������о��������о�������£�

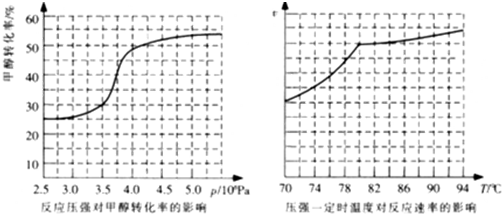
�ٴӷ�Ӧѹǿ�Լ״�ת���ʵ�Ӱ�조Ч��"������ҵ��ȡ�������Ӧѡ���ѹǿ�� ��
��ʵ�ʹ�ҵ�����в��õ��¶���80�棬�������� ��
��1��ac
��2��COһ2eһ+O2һ=CO2
��3���ٸ÷�Ӧ��H<0
��2CO(g)+2H2(g)  CH4(g)+C02(g) ��H=-247.6 kJ��mol-1
CH4(g)+C02(g) ��H=-247.6 kJ��mol-1
��4����3.5��106 Pa��4.0��106 Pa
�ڸ���80��ʱ���¶ȶԷ�Ӧ����Ӱ���С���ҷ�Ӧ���ȣ������¶�ʱƽ�������ƶ���ת���ʽ���
(ÿ��2�֣����12��)
��������
�����������1�������������ƽ�⡱���淴Ӧ������ϵ��ѹǿ���ܶȣ���������������仯�����DZ�����b�����ʵ�Ũ�Ȳ�����ƽ���־�������ֻ��һ���ض�״̬�������ԣ�d��CO������������H2�������������ͬ��һ����ȣ���2������COʧȥ���ӣ�����CO2��COһ2eһ+O2һ=CO2
����3���ٸ÷�Ӧ�ġ�S<0��ֻ�ܡ�H<0�����Է����У���2CO(g)+2H2(g)  CH4(g)+C02(g) ��H=-247.6 kJ��mol-1����4������ͼ��֪����ѹǿ�ﵽ4.0��106 Paѹǿ��ת���ʵ�Ӱ���С���ʹ�ҵ��ȡ�������Ӧѡ���ѹǿ��3.5��106 Pa��4.0��106 Pa������ͼ�۲��֪�¶ȸ���80��ʱ���¶ȶԷ�Ӧ����Ӱ���С���ҷ�Ӧ���ȣ������¶�ʱƽ�������ƶ���ת���ʽ��͡�
CH4(g)+C02(g) ��H=-247.6 kJ��mol-1����4������ͼ��֪����ѹǿ�ﵽ4.0��106 Paѹǿ��ת���ʵ�Ӱ���С���ʹ�ҵ��ȡ�������Ӧѡ���ѹǿ��3.5��106 Pa��4.0��106 Pa������ͼ�۲��֪�¶ȸ���80��ʱ���¶ȶԷ�Ӧ����Ӱ���С���ҷ�Ӧ���ȣ������¶�ʱƽ�������ƶ���ת���ʽ��͡�
���㣺���黯ѧ��Ӧԭ�����漰ƽ���־���жϡ��缫��Ӧʽ��д���Ȼ�ѧ����ʽ��д����Ӧ������ѡ����й����⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� |
| ���� |
| C7(N2)C12(H2O) |
| C6(NO2)C8(NH3) |
| C7(N2)C12(H2O) |
| C6(NO2)C8(NH3) |
| ��Ӧʱ��/min | n��CO��/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| 0.2 |
| t1 |
| 0.2 |
| t1 |
| �ⶨʱ��/h | 0 | 1 | 2 | 3 | 4 |
| ��ˮ��Ʒ��pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ���¸�ѹ |
| ||
| ���¸�ѹ |
 CO��g��+3H2��g������H=+QkJ/mol��Q��0��
CO��g��+3H2��g������H=+QkJ/mol��Q��0��| ʱ��/min | CH4��mol�� | H20�� mol�� | CO ��mol�� | H2 ��mol�� |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | X1 | X2 | X3 | 0.60 |
| 7 | Y1 | Y2 | 0.20 | Y3 |
| 10 | 0.21 | 0.81 | 0.19 | 0.62 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
(��12��)�����������ɫֲ��������������������ù����ɼ�����ϳɸ��ܸ��ӷ��ӵĹ��̡����������Ҷ���ط����������ø��������(MS)���ϣ�����һϵ��������ԭ��Ӧ����ѧ���Ƿ��ֹ�����û���������仯��ʽ������Щϸ������H2S����H2O���й���������ɽṹ��������ȫ���ƵIJ��
�ҹ���ѧ������1946��ͷ������������Ӻ�ɷ������ѱ���ѳɽ�С����Ƭ������һ�������Ӻ��![]() �������ѱ�ʱ���ܲ������ֺ���72X��
�������ѱ�ʱ���ܲ������ֺ���72X��![]() �����ɿ����ӡ��������������72X��Ӧ������
�����ɿ����ӡ��������������72X��Ӧ������![]() ���̶���������MS�н���M��һ�ֺ��ء�M��Ӧ����㷺�Ľ���֮һ���ڸ��¸�ѹ����CO�������ɵ���ɫҺ��A(A�ڸ����¿ɷֽ�ΪM��CO)������M��һ�����ɫ�����ᄃ��B����˳���ԣ��ڼ�����Һ��B�ܰ�Cr(��)����ΪCrO42-������������ԭ��C����Һ��C�ɱ�����������B������C�ڸ����¿ɷֽ⣬�����Ϊ̼����D���綾�ļ���E�ͻ�ѧ��������F��A������CO���ÿ��γ�����18���ӹ���Ľ����л�������M2(CO)9��(18���ӹ���ָ���ɽ����л��������У������ļ۵��Ӻ������ṩ�����ĵ�����������18)��
���̶���������MS�н���M��һ�ֺ��ء�M��Ӧ����㷺�Ľ���֮һ���ڸ��¸�ѹ����CO�������ɵ���ɫҺ��A(A�ڸ����¿ɷֽ�ΪM��CO)������M��һ�����ɫ�����ᄃ��B����˳���ԣ��ڼ�����Һ��B�ܰ�Cr(��)����ΪCrO42-������������ԭ��C����Һ��C�ɱ�����������B������C�ڸ����¿ɷֽ⣬�����Ϊ̼����D���綾�ļ���E�ͻ�ѧ��������F��A������CO���ÿ��γ�����18���ӹ���Ľ����л�������M2(CO)9��(18���ӹ���ָ���ɽ����л��������У������ļ۵��Ӻ������ṩ�����ĵ�����������18)��
(1) M��Ԫ�ط���Ϊ ��B�Ļ�ѧʽΪ ��
(2) д���������к˻�ѧ��Ӧ����ʽ��
(3) д��B��Cr(��)����ΪCrO42-�����ӷ���ʽ��
(4) H2S����H2O���й�����õ���Ҫ������ ���÷�Ӧ�ܹ���������Ҫԭ���ǣ� ��
(5) ָ��M2(CO)9�й��м��ֲ�ͬ�ijɼ���ʽ������M2(CO)9�Ľṹʽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com