
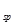 :
: | 物质 | 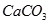 | 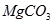 | 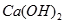 | 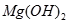 |
| 溶度积 | 2.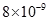 | 6.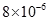 | 5.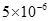 | 1.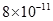 |
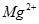 转化为
转化为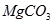 沉淀,并解释原因: 。
沉淀,并解释原因: 。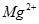 转化为
转化为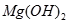 沉淀,而不是转化为
沉淀,而不是转化为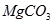 沉淀,其理由是 ;请你推测应将贝壳进行怎样的加工处理 。
沉淀,其理由是 ;请你推测应将贝壳进行怎样的加工处理 。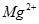 转化为
转化为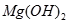 沉淀,理由是 。
沉淀,理由是 。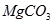 的溶解度比
的溶解度比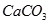 溶解度大,直接加贝壳粉末得不到
溶解度大,直接加贝壳粉末得不到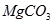 沉淀(2分)
沉淀(2分)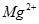 沉淀完全,应将
沉淀完全,应将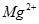 转化为溶解度更小的
转化为溶解度更小的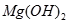 ;(2分)研磨、煅烧、加水制成石灰乳。(2分)
;(2分)研磨、煅烧、加水制成石灰乳。(2分)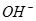 能结合
能结合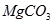 溶解产生的
溶解产生的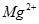 生成溶解度更小的
生成溶解度更小的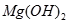 沉淀,使?
沉淀,使?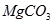 ?的沉淀溶解平衡不断向右移动。(2分)
?的沉淀溶解平衡不断向右移动。(2分)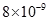 < 6.
< 6.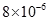 ,
,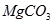 的溶解度比
的溶解度比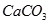 溶解度大,直接加贝壳粉末得不到
溶解度大,直接加贝壳粉末得不到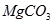 沉淀.
沉淀.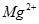 沉淀完全,应将
沉淀完全,应将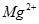 转化为溶解度更小的
转化为溶解度更小的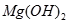 ;(2分)应将贝壳研磨、煅烧、加水制成石灰乳。CaCO3=CaO+CO2↑ CaO+H2O="Ca" (OH)2 Mg2++2OH―="Mg" (OH)2↓
;(2分)应将贝壳研磨、煅烧、加水制成石灰乳。CaCO3=CaO+CO2↑ CaO+H2O="Ca" (OH)2 Mg2++2OH―="Mg" (OH)2↓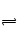 Mg(OH)2+CO32― ,烧碱电离产生的
Mg(OH)2+CO32― ,烧碱电离产生的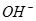 能结合
能结合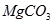 溶解产生的
溶解产生的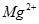 生成溶解度更小的
生成溶解度更小的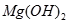 沉淀,使?
沉淀,使?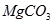 ?的沉淀溶解平衡不断向右移动。
?的沉淀溶解平衡不断向右移动。

科目:高中化学 来源:不详 题型:实验题

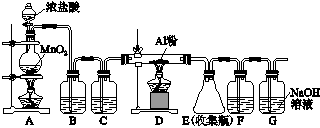
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
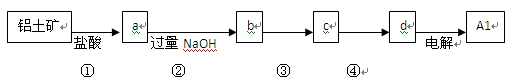
| A.①、②中除加试剂外。还需要进行过滤操作 |
| B.a 、b中铝元素的化合价相同 |
| C.③中需要通入过量的氨气 |
| D.④进行的操作是加热,而且d 一定是氧化铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,铝和浓硫酸、浓硝酸不反应。 |
| B.两份相同质量的铝粉,分别与足量的稀硫酸和氢氧化钠溶液反应生成的氢气前者多。 |
| C.合金的熔点一般比组成的金属成分的熔点都低 |
| D.用酒精灯加热一小片铝箔,熔化的铝会滴落 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,含有杂质
,含有杂质 、
、 、
、 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程: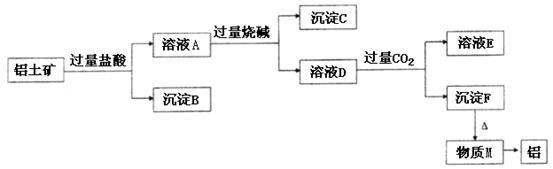
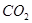 生成沉淀F的离子方程式为________________________。
生成沉淀F的离子方程式为________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
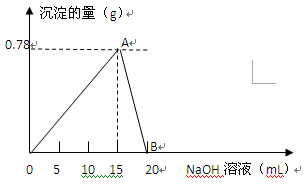
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.先生成沉淀,后沉淀全部溶解 |
| B.当溶液中Al3+全部沉淀出来时,沉淀的总物质的量最大 |
| C.最后得到的沉淀是BaSO4 |
| D.最后的沉淀为2mol BaSO4、1mol Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
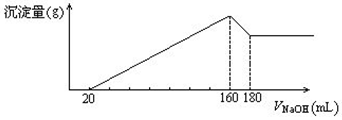
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com