��a molO
2��b mol SO
2�������һ�ܱ������У����������·�����ӦO
2+2SO
2?2SO
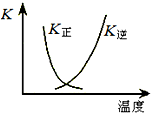
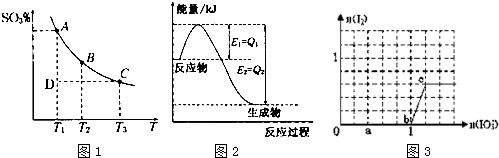
3��1��ͼ�����߱�ʾ������Ӧ�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯����������Ӧ����ӦΪ
��Ӧ��������ȡ����ȡ���
��2��������Ӧ��ƽ���SO
2��O
2��SO
3�����ʵ���֮��Ϊ3��4��6�����������������䣬�����¶Ⱥ�ﵽ�µ�ƽ��ʱ��O
2��SO
3�����ʵ����ֱ���1.1mol��2.0mol����ʱ������SO
2�����ʵ���Ӧ��
mol
����Ҫʹƽ��ʱ��Ӧ��������ʵ�����������������ʵ�����ȣ���a��b֮��kӦ����
A��1��
��3 B��
��
��
C��3��
��4 D��
��
��
��3������ͬ�¶��£�������Ӧ�����������ͬ�ļס������������У�a=b����ƽ������У��ױ���������䣬�ұ���ѹǿ���䣬������SO
2��ת����Ϊp%��������SO
2��ת����
p% �����������������=����
��4��Li-SOCl
2��س�����������������缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl
4-SOCl
2����ص��ܷ�ӦΪ��4Li+2SOCl
2=4LiCl+S+SO
2��������������ĵ缫��ӦʽΪ
��
��5��0.1mol/LKHSO
4��0.1mol/LNa
2S��Һ�������Ϻ���Һ��ʹpH��ֽ��������c��S
2-��+c��H
2S��+c��HS
-��+c��SO
42-��=
mol/L������H
2S���岻�ݳ���
��6��Ҫʹ������0.2mol?L
-1CuSO
4��Һ��Cu
2+������Ϊ��ȫ��ʹCu
2+Ũ�Ƚ���ԭ����ǧ��֮һ������Ӧ����Һ�����NaOH��Һ��ʹ��Һ��pH��
��K
sp Cu��OH��
2=2��10
-20��

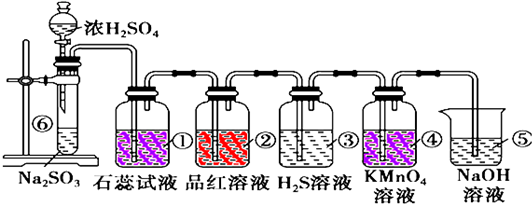
 ��a molO2��b mol SO2�������һ�ܱ������У����������·�����ӦO2+2SO2?2SO3
��a molO2��b mol SO2�������һ�ܱ������У����������·�����ӦO2+2SO2?2SO3


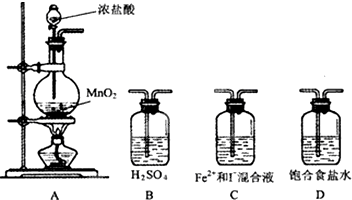 ij�о���ѧϰС�����뽫����Cl2ͨ��Fe2+��I-�Ļ����Һ����̽��Fe2+��I-�Ļ�ԭ��ǿ����
ij�о���ѧϰС�����뽫����Cl2ͨ��Fe2+��I-�Ļ����Һ����̽��Fe2+��I-�Ļ�ԭ��ǿ����