
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. 0.1 mol•L﹣1 (NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl﹣、MnO4﹣
B. 0.1 mol•L﹣1 FeCl2溶液:K+、Na+、SO42﹣、NO3﹣
C. 使甲基橙变红色的溶液:NH4+、Cu2+、ClO﹣、Cl﹣
D. 0.1mol•L﹣1NaHCO3溶液:K+、AlO2﹣、Cl﹣、NO3﹣
考点: 离子共存问题.
分析: A.(NH4)2Fe(SO4)2电离出亚铁离子,高锰酸根离子能够氧化亚铁离子;
B.四种离子之间不反应,都不与氯化亚铁反应;
C.使甲基橙变红色的溶液中存在大量氢离子,次氯酸根离子与氢离子反应生成次氯酸;
D.碳酸氢根离子的酸性大于氢氧化铝,碳酸氢钠与偏铝酸根离子反应生成氢氧化铝沉淀.
解答: 解:A.(NH4)2Fe(SO4)2电离出的亚铁离子具有还原性,能够被MnO4﹣氧化,在溶液中不能大量共存,故A错误;
B.K+、Na+、SO42﹣、NO3﹣之间不发生反应,都不与FeCl2反应,在溶液中能够大量共存,故B正确;
C.使甲基橙变红色的溶液为酸性溶液,溶液中存在大量氢离子,ClO﹣与氢离子结合生成次氯酸,在溶液中不能大量共存,故C错误;
D.碳酸氢根离子的酸性大于氢氧化铝,NaHCO3与AlO2﹣反应生成氢氧化铝沉淀和碳酸钠,在溶液中不能大量共存,故D错误;
故选B.
点评: 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH﹣;是“可能”共存,还是“一定”共存等.


科目:高中化学 来源: 题型:
COCl2(g)⇌CO(g)+Cl2(g);△H>0.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
|
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关C、N、S等非金属元素化合物的说法正确的是( )
A.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
B.SO2具有漂白性可以使酸性高锰酸钾溶液褪色
C.实验室可用NaOH溶液处理NO2和SO2废气
D.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L的密闭容器中进行反应:3H2+N2 2NH3,经过一段时间后,NH3的物质的量增加0.8mol,在这段时间内用N2表示的平均反应速率为0.01mol•l﹣1•s﹣1.则这段时间为()
2NH3,经过一段时间后,NH3的物质的量增加0.8mol,在这段时间内用N2表示的平均反应速率为0.01mol•l﹣1•s﹣1.则这段时间为()
A. 10s B. 20s C. 30s D. 40s
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是()
A. 氯化钙的电子式: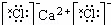
B. 168O2﹣离子的结构示意图: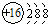
C. H2CO3的电离方程式:H2CO3⇌2H++CO32﹣
D. 葡萄糖的结构简式:C6H12O6
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界中存在一种尖晶石,主要成分的化学式可表示为MgA12O4,可作为宝石.已知该尖晶石中混有Fe2O3.取5.4g样品,恰好完全溶解在100mL一定浓度的盐酸中,则该盐酸的浓度可能是()
A. 1.8mol/L B. 2.8mol/L C. 4.3mol/L D. 4.9mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知,将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3 ,且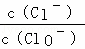 的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
A. 若某温度下,反应后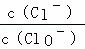 =11,则溶液中
=11,则溶液中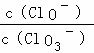 =
=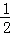
B. 参加反应的氯气的物质的量小于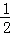 a mol
a mol
C. 改变温度,反应中转移电子的物质的量ne的范围: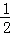 a mol≤ne≤
a mol≤ne≤ a mol
a mol
D. 改变温度,产物中KC1O3的最大理论产量为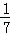 a mol
a mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com