
利用I2O5可消除CO污染,反应为5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
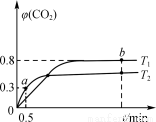
A.T1<T2,ΔH>0
B.T1温度下,该反应的平衡常数为1 024
C.T2温度下,0~0.5 min内,CO的平均反应速率为0.3 mol·L-1·min-1
D.T1温度下,若向装有足量I2固体的2 L恒容密闭容器中通入10 mol CO2,达到平衡时,φ(CO2)=0.8
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下图是氢氧燃料电池(电解质溶液为H3PO4溶液)构造示意图。关于该电池的说法不正确的是
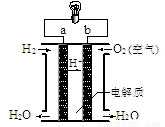
A.a极是负极
B.电子由a通过灯泡流向b
C.正极的电极反应是:O2+2H2O+4e-=4OH-
D.氢氧燃料电池是环保电池
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)一定条件下,在一容积为4 L的密闭容器中通入0.4 molN2和1.2 molH2,发生反应:N2(g)+3H2(g) 2NH3(g) △H<0;
2NH3(g) △H<0;
(1)当进行到第4分钟时达到平衡,生成NH3为0.4 mol,则从开始到达平衡时NH3的平均速率v(NH3)=_____________(注明单位)。
(2)该条件下,反应的平衡常数表达式K = ______ ,若降低温度,K值将_____(填“增大”“减小”“不变”)
(3)达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将_____移动(“向逆反应方向”、“向正反应方向”或“不”).
(4)在三个相同的容器中各充入1 molN2和3molH2,在不同条件下分别达到平衡,氨的体积分数随时间变化如图。下列说法正确的是 。
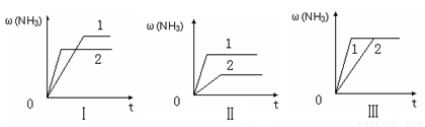
a.图Ⅰ可能是不同压强对反应的影响,且P2>P1
b.图Ⅱ可能是不同温度对反应的影响,且T1>T2
c.图Ⅲ可能是同温同压下,催化剂性能,1>2
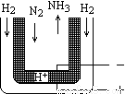
(5)常压下,把H2和用氦气(He)稀释的N2分别通入一个加热到570℃的电解池装置,H2和N2便可在电极上合成氨,装置中所用的电解质(图中黑细点)能传导H+,则阴极的电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示。已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是
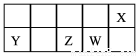
A.X分别与Y、Z形成的化合物中化学键类型相同
B.Z的最高价氧化物的对应水化物酸性比W的强
C.X的简单气态氢化物的稳定性比W的弱
D.原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:填空题
(14分)大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放。
(1)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
N2(g)+O2(g)===2NO(g);ΔH=+180 kJ·mol-1
CH4可用于脱硝,其热化学方程式为CH4(g)+4NO(g)===CO2(g)+2N2(g)+2H2O(l),ΔH=________。
(2)C2H4也可用于烟气脱硝。为研究温度、催化剂中Cu2+负载量对其NO去除率的影响,控制其他条件一定,实验结果如图1所示。为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是________。
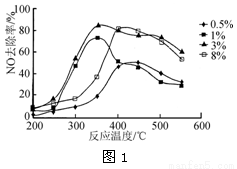

(3)臭氧也可用于烟气脱硝。
①O3氧化NO结合水洗可产生HNO3和O2,该反应的化学方程式为____。
②一种臭氧发生装置原理如图2所示。阳极(惰性电极)的电极反应式为________。
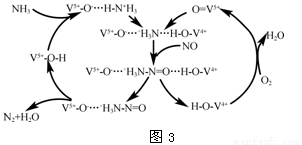
(4)图3是一种用NH3脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为________(填化学式)和H2O。
②当消耗2 mol NH3和0.5 mol O2时,除去的NO在标准状况下的体积为________。

(5)NO直接催化分解(生成N2与O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40 ℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图4所示。写出Y和Z的化学式:____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
一种三室微生物燃料电池污水净化系统原理如右图所示,图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是
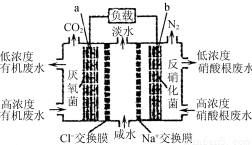
A.b电极为该电池的负极
B.b电极附近溶液的pH减小
C.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
D.中间室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1NH4HCO3溶液:K+、Na+、SO42-、OH-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.0.1 mol·L-1CH3COONa溶液:Mg2+、H+、Cl-、SO42-
D.Kw/c(H+)=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市高三3月月考化学试卷(解析版) 题型:填空题
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题:
(1)元素D在周期表中的位置_______________________。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)___________.
(3)由A、B、C三种元素以原子个数比4 :2 :3形成化合物X,X中所含化学键类型有______________.
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:____________;若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:________________。
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为: ,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
,乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
A.与HCl加成生成CH3COCl
B.与H2O加成生成CH3COOH
C.与CH3OH加成生成CH3COCH2OH
D.与CH3COOH加成生成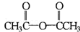
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com