
| A£® | ³£ĪĀĻĀ£¬½«pH=3µÄ“×ĖįČÜŅŗĻ”ŹĶµ½ŌĢå»żµÄ10±¶ŗó£¬ČÜŅŗµÄpH=4 | |
| B£® | ĪŖČ·¶ØijĖįH2AŹĒĒæĖį»¹ŹĒČõĖį£¬æɲāNaHAČÜŅŗµÄpH£¬ČōpH£¾7£¬ŌņH2AŹĒČõĖį£»ČōpH£¼7£¬ŌņH2AŹĒĒæĖį | |
| C£® | ÓĆ0.2000 mol/L NaOH±ź×¼ČÜŅŗµĪ¶ØHClÓėCH3COOHµÄ»ģŗĻČÜŅŗ£Ø»ģŗĻŅŗÖŠĮ½ÖÖĖįµÄÅØ¶Č¾łŌ¼ĪŖ0.1 mol/L£©£¬ÖĮÖŠŠŌŹ±£¬ČÜŅŗÖŠµÄĖįĪ“±»ĶźČ«ÖŠŗĶ | |
| D£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬½«×ćĮæĀČ»ÆŅų¹ĢĢå·Ö±š·ÅČėĻąĶ¬Ģå»żµÄ¢ŁÕōĮóĖ®”¢¢Ś0.1mol/LŃĪĖį”¢¢Ū0.1 mol/LĀČ»ÆĆ¾ČÜŅŗ”¢¢Ü0.1mol/LĻõĖįŅųČÜŅŗÖŠ£¬Ag+ÅØ¶Č£ŗ¢Ł£¾¢Ü=¢Ś£¾¢Ū |
·ÖĪö A£®“×ĖįŹĒČõµē½āÖŹ£¬ŌŚĖ®ČÜŅŗÖŠ“ęŌŚµēĄėĘ½ŗā£¬¼ÓĖ®Ļ”ŹĶ“Ł½ų“×ĖįµēĄė£»
B£®NaHAĖ®ČÜŅŗpH£¼0Ź±£¬H2AæÉÄÜŹĒČõĖįŅ²æÉÄÜŹĒĒæĖį£»
C£®“×ĖįÄĘŹĒĒæ¼īČõĖįŃĪ£¬ĘäĖ®ČÜŅŗ³Ź¼īŠŌ£¬ŅŖŹ¹“×ĖįŗĶNaOHµÄĖ®ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ“×ĖįÓ¦øĆÉŌĪ¢¹żĮ棻
D£®AgClÄŃČÜŅŗĖ®£¬ŌŚĖ®ČÜŅŗÖŠ“ęŌŚČܽāĘ½ŗā£¬Čē¹ūČÜŅŗÖŠŗ¬ÓŠAg+»ņCl-£¬»įŅÖÖĘAgClČܽā£¬ĻõĖįŅųŹĒæÉČÜŠŌŅųŃĪ£®
½ā“š ½ā£ŗA£®“×ĖįŹĒČõµē½āÖŹ£¬ŌŚĖ®ČÜŅŗÖŠ“ęŌŚµēĄėĘ½ŗā£¬¼ÓĖ®Ļ”ŹĶ“Ł½ų“×ĖįµēĄė£¬ĖłŅŌ³£ĪĀĻĀ£¬½«pH=3µÄ“×ĖįČÜŅŗĻ”ŹĶµ½ŌĢå»żµÄ10±¶ŗó£¬ČÜŅŗÖŠĒāŌ×ÓÅØ¶Č“óÓŚŌĄ“µÄ$\frac{1}{10}$£¬ĖłŅŌøĆČÜŅŗµÄpH£¼4£¬¹ŹA“ķĪó£»
B£®NaHAĖ®ČÜŅŗpH£¼0Ź±£¬H2AæÉÄÜŹĒČõĖįŅ²æÉÄÜŹĒĒæĖį£¬ČēNaHSO3ČÜŅŗpH£¼7£¬µ«H2SO3ŹĒČõĖį£¬NaHSO4ČÜŅŗpH£¼7£¬µ«H2SO4ŹĒĒæĖį£¬¹ŹB“ķĪó£»
C£®“×ĖįÄĘŹĒĒæ¼īČõĖįŃĪ£¬ĘäĖ®ČÜŅŗ³Ź¼īŠŌ£¬ŅŖŹ¹“×ĖįŗĶNaOHµÄĖ®ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ“×ĖįÓ¦øĆÉŌĪ¢¹żĮ棬ĖłŅŌÓĆ0.2000 mol/L NaOH±ź×¼ČÜŅŗµĪ¶ØHClÓėCH3COOHµÄ»ģŗĻČÜŅŗ£Ø»ģŗĻŅŗÖŠĮ½ÖÖĖįµÄÅØ¶Č¾łŌ¼ĪŖ0.1 mol/L£©£¬ÖĮÖŠŠŌŹ±£¬ĖįÓŠŹ£Óą£¬ĖłŅŌČÜŅŗÖŠµÄĖįĪ“±»ĶźČ«ÖŠŗĶ£¬¹ŹCÕżČ·£»
D£®AgClÄŃČÜŅŗĖ®£¬ŌŚĖ®ČÜŅŗÖŠ“ęŌŚČܽāĘ½ŗā£¬Čē¹ūČÜŅŗÖŠŗ¬ÓŠAg+»ņCl-£¬»įŅÖÖĘAgClČܽā£¬
ĀČĄė×ÓÅضČŌ½“óŅÖÖĘAgClČܽā³Ģ¶ČŌ½“ó£¬ĻõĖįŅųŹĒæÉČÜŠŌŅųŃĪ£¬ŅųĄė×ÓÅضČ×ī“ó£¬ĖłŅŌÕā¼øÖÖČÜŅŗÖŠAg+ÅØ¶Č£ŗ¢Ü£¾¢Ł£¾¢Ś£¾¢Ū£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éČõµē½āÖŹµÄµēĄė¼°Ąė×ÓÅØ¶Č“óŠ”±Č½ĻµČÖŖŹ¶µć£¬Ć÷Č·Čõµē½āÖŹµēĄėĢŲµć¼°ÄŃČÜĪļČܽāĘ½ŗāÓ°ĻģŅņĖŲŹĒ½ā±¾Ģā¹Ų¼ü£¬ŅדķŃ”ĻīŹĒD£¬×¢Ņā£ŗĖäČ»ĻõĖįŅųŅÖÖĘAgClČܽā£¬µ«ĻõĖįŅųŹĒæÉČÜŠŌĪļÖŹ£¬ĢāÄæÄѶČÖŠµČ£®


 æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Įņ»ÆŃĒĢśÓėĻ”ĻõĖį·“Ó¦£ŗFeS+2H+”śFe2++H2S | |
| B£® | “æ¼īČÜŅŗÖŠµĪ¼ÓÉŁĮæŃĪĖį£ŗCO32-+H+”śHCO3- | |
| C£® | ¹żĮæµÄNaHSO4ÓėBa£ØOH£©2ČÜŅŗ·“Ó¦£ŗBa2++2OH-+2H++SO42-”śBaSO4”ż+2H2O | |
| D£® | ½«ÉŁĮæSO2ĘųĢåĶØČėCa£ØClO£©2ČÜŅŗÖŠ£ŗSO2+Ca2++2ClO-+H2O”śCaSO3”ż+2HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ł¢Ū¢Ü¢Ż¢Ž | C£® | ¢Ł¢Ū¢Ž | D£® | ¢Ł¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
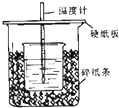 ÓĆ50mL0.50mol/LŃĪĖįÓė50mL0.55mol/LNaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ÓĆ50mL0.50mol/LŃĪĖįÓė50mL0.55mol/LNaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØNa+£©£¾c£ØHCO3-£©£¾c£ØH+£©£¾c£ØOH-£© | B£® | c£ØNa+£©=c£ØHCO3-£©£¾c£ØOH-£©£¾c£ØH+£© | ||
| C£® | c£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+2c£ØCO32-£© | D£® | c£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+c£ØCO32-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
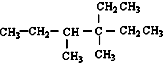 ŹĒÓÉijµ„Ļ©ĢžÓėH2¼Ó³ÉŗóµÄ²śĪļ£¬æ¼ĀĒĻ©ĢžµÄĖ³·“Ņģ¹¹£¬ŌņÕāÖÖµ„Ļ©ĢžµÄ½į¹¹æÉÄÜÓŠ£Ø””””£©
ŹĒÓÉijµ„Ļ©ĢžÓėH2¼Ó³ÉŗóµÄ²śĪļ£¬æ¼ĀĒĻ©ĢžµÄĖ³·“Ņģ¹¹£¬ŌņÕāÖÖµ„Ļ©ĢžµÄ½į¹¹æÉÄÜÓŠ£Ø””””£©| A£® | 3ÖÖ | B£® | 4 | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³żČ„Cu2+ÖŠµÄÉŁĮæFe3+£¬æɼÓČėCuO | |
| B£® | ·Šµć£ŗ¾§Ģå¹č£¾SiO2£¾SiCl4£¾NaCl | |
| C£® | Cu£ØNH3£©${\;}_{4}^{2+}$ÖŠµÄÅäĪ»¼üŹĒÓÉCu2+Ģį¹©¹Ā¶Ōµē×Ó£¬NH3Ģį¹©æÕ¹ģµĄŠĪ³ÉµÄ | |
| D£® | ŹÆÓĶµÄ·ÖĮó”¢ĆŗµÄŅŗ»ÆŅŌ¼°ĆŗµÄøÉĮóµČÉś²ś¹ż³ĢÖŠ¾łÖ»·¢ÉśĪļĄķ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C5H12 | B£® | C4H10 | C£® | C3H6 | D£® | C3H8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĶÖ¬Ė®½āæɵƵ½±ūČż“¼ | |
| B£® | æÉÓƵā¼ģŃéµķ·ŪŹĒ·ń·¢ÉśĖ®½ā | |
| C£® | µ°°×ÖŹĖ®½āµÄ×īÖÕ²śĪļ¾łĪŖ°±»łĖį | |
| D£® | ĻĖĪ¬ĖŲĖ®½āÓėµķ·ŪĖ®½āµĆµ½µÄ×īÖÕ²śĪļĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com