
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源:不详 题型:单选题
| A.通入H2的电极为负极, 其电极反应式是: H2+2OH-→2H2O+2e- |
| B.正极的电极反应式是:O2+2H2O+4e-→ 4OH-,发生氧化反应 |
| C.燃料电池工作时溶液中的阴离子向负极移动 |
| D.该电池放电时,每反应1mol氢气将转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①式表示负极反应,②式表示正极反应 |
| B.铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低 |
| C.铅蓄电池在放电时,电子从Pb通过导线流向PbO2 |
| D.铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42―–2e―=PbSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Y为CuSO4溶液 |
| B.正极反应为Cu-2e- = Cu2+ |
| C.在外电路中,电流从Cu极流向Ag极 |
| D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C2H5OH在电池的负极上参加反应 |
| B.1mol乙醇被氧化转移6mol电子 |
| C.在外电路中电子由负极沿导线流向正极 |
| D.电解质溶液中阳离子移向正极,阴离子移向负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Ni(OH)2+2Cd (OH)2 已知Ni(OH)2和Cd (OH)2均难溶于水但能溶于酸,以下说法中正确的是
2Ni(OH)2+2Cd (OH)2 已知Ni(OH)2和Cd (OH)2均难溶于水但能溶于酸,以下说法中正确的是| A.①③ | B.②④ | C.①④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌外壳是负极,石墨碳棒是正极材料 | B.在外电路中电子从碳棒流向锌外壳 |
| C.电流从锌流到碳棒上 | D.在电池内部阳离子从碳棒向锌片移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铅蓄电池在放电过程中,负极质量最终减小,正极质量最终增加 |
| B.放热反应不一定能自发进行 |
| C.一定条件下,使用催化剂能加快反应速率,但不能提高反应物的平衡转化率 |
| D.温度一定,当溶液中Ag+和Cl-浓渡的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

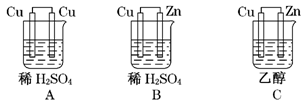
 的顺序是________。
的顺序是________。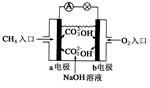
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com