
| A. | ②③④⑦⑧ | B. | ②③④⑥⑦ | C. | ③④⑥⑦⑧ | D. | ①②③④⑤ |
分析 在相同条件下,气体的Vm相等,物质的量相同的两种气体,气体的分子数相等,体积相等,根据N=nNA、m=nM、ρ=$\frac{M}{{V}_{m}}$分子构成进行解答该题.
解答 解:在相同条件下,气体的Vm相等,物质的量相同的两种气体,分子数相等,
①根据N=nNA可知,物质的量相同的两种气体,分子数相等,故①不选;
②根据ρ=$\frac{M}{{V}_{m}}$知,相同条件下,密度与其摩尔质量成正比,摩尔质量不一定相等,所以其密度不一定相等,故②选;
③相同条件下,物质的量相同的两种气体,摩尔质量不一定相等,如O2和O3,故③选;
④根据m=nM知,物质的量相等,其质量与摩尔质量成正比,摩尔质量不一定相等,所以其质量不一定相等,故④选;
⑤同温同压下,气体摩尔体积相等,体积相等,故⑤不选;
⑥同温同压下,气体摩尔体积相等,故⑥不选;
⑦每个分子含有的原子数目不一定相同,故二者含有原子数不一定相等,如O2和O3,故⑦选;
⑧两种气体分子中质子数不一定相等,则电子数不一定相等,分子数相等,所以其电子数不一定相等,故⑧选;
故选A.
点评 本题考查阿伏加德罗定律及其推论,为高考常见题型,侧重于学生的分析能力的考查,答题时注意能举出实例,把握相关计算公式,题目难度不大.


科目:高中化学 来源: 题型:解答题
| ① | HF | Ka=6.8×10-4 mol•L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol•L-1 |
| ③ | HCN | Ka=6.2×10-10 mol•L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol•L-1 Ka2=4.7×10-11 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
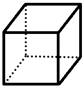 “立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示.
“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
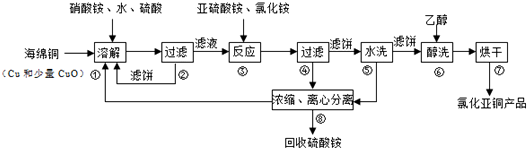
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质铁与水蒸气的反应 | B. | 铝片与氢氧化钠溶液的反应 | ||
| C. | 过氧化钠与二氧化碳的反应 | D. | 碳酸钠溶液与稀盐酸的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
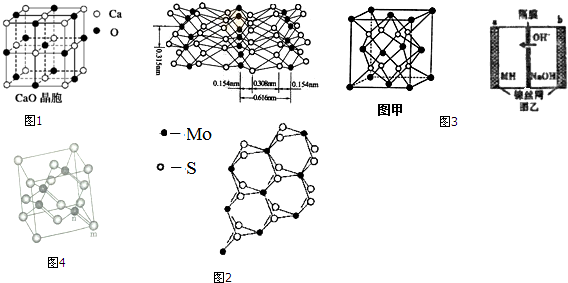
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ |
| 0.1mol/L 盐酸 | pH=3 盐酸 | 0.1mol/L 氨水 | pH=11 氨水 |
| A. | 由水电离出的c(H+):①>③ | |
| B. | ③稀释到原来的100倍后,pH与④相同 | |
| C. | ①与③混合,若溶液pH=7,则V(盐酸)>V(氨水) | |
| D. | ②与④混合,若溶液显碱性,则所得溶液中离子浓度可能为:c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com