
 如下表是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题
如下表是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题 | ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
分析 由元素在周期表中位置,可知①为H、②为B、③为C、④为N、⑤为O、⑥为F、⑦为Fe、⑧为Cu、⑨为Zn.
(1)①为H,核外电子排布为1s1;
(2)②、⑥两元素形成的化合物为BF3,计算B原子孤电子对数、价层电子对数,确定空间构型与B原子杂化方式;
(3)元素⑧为Cu,核外电子数为29,根据核外电子排布规律书写基态原子的电子排布式;
(4)N元素原子2p能级为半满稳定结构,能量较低,第一电离能高于同周期相邻元素;同周期自左而右元素电负性增大;
(5)元素⑦与CO可形成的Fe(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,熔沸点低,易溶于非极性溶剂,属于分子晶体;
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中生成配离子;
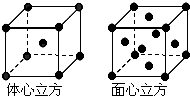
(7)根据均摊法计算面心立方晶胞和体心立方晶胞中实际含有的原子个数之比.
解答 解:由元素在周期表中位置,可知①为H、②为B、③为C、④为N、⑤为O、⑥为F、⑦为Fe、⑧为Cu、⑨为Zn.
(1)①为H,核外电子排布为1s1,处于周期表中s区,故答案为:s;
(2)②、⑥两元素形成的化合物为BF3,B原子孤电子对数为0、价层电子对数3,空间构型为平面正三角形,B原子杂化方式为sp2杂化,
故答案为:平面正三角形;sp2;
(3)元素⑧为Cu,核外电子数为29,基态原子的电子排布式为1s22s22p63s23p63d104s1,
故答案为:1s22s22p63s23p63d104s1;
(4)N元素原子2p能级为半满稳定结构,能量较低,第一电离能高于同周期相邻元素,故第一电离能C<N;同周期自左而右元素电负性增大,故电负性N<O,
故答案为:<;<;
(5)元素⑦与CO可形成的Fe(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,熔沸点低,易溶于非极性溶剂,属于分子晶体,
故答案为:分子;
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中生成配离子,Zn2+离子与NH3间结合的作用力为配位键,
故答案为:配位键;
(7)面心立方晶胞中实际含有的原子个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,体心立方晶胞中实际含有的原子个数为1+8×$\frac{1}{8}$=2,二者含有原子数目之比为4:2=2:1,
故答案为:2:1.
点评 本题是对物质结构与性质的考查,涉及元素周期表、核外电子排布、空间构型与杂化方式判断、电离能、电负性、晶体类型与性质、配合物、晶胞计算等,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 生成物都属于电解质 | |
| B. | HCl全部发生氧化反应 | |
| C. | 该反应表明氧化性KClO3比Cl2强 | |
| D. | 1 mol KClO3在反应中得到6 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在测定中和反应的反应热实验中,只要读一次温度 | |
| B. | 可用pH试纸测定新制氯水的pH | |
| C. | 中和滴定实验中,洗净后的锥形瓶不需要干燥 | |
| D. | 向CH3COONa溶液中滴入石蕊试液,溶液变蓝 | |
| E. | 向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaHCO3固体加入新制氯水,有无色气泡(H) | |
| B. | 使红色布条褪色(HCl) | |
| C. | 向氯水中加入CuSO4,变蓝色,(H2O) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | 氢氧化钡溶液与硫酸反应:OHˉ+SO42-+Ba2++H+═H2O+BaSO4 | |
| C. | 二氧化硅与氢氧化钠溶液反应:SiO2+OHˉ═H2SiO3 | |
| D. | 碳酸钙与盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O═Ca(OH)2 | |
| B. | Zn+2HCl═ZnCl2+H2↑ | |
| C. | NaCl+AgNO3═AgCl+NaNO3 | |
| D. | 2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下水电离出的c(H+)•c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- | |
| B. | 无色溶液中:K+、CH3COO-、HCO3-、MnO4- | |
| C. | 不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2- | |
| D. | 中性透明溶液:K+、Cl-、NO3-、Fe3+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
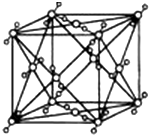 已知A、B、C、D、E都是周期表中的前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外层电子层的P能级(轨道)上的电子处于半充满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一类半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.
已知A、B、C、D、E都是周期表中的前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外层电子层的P能级(轨道)上的电子处于半充满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一类半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com