
| A. | 升高温度,v(正)变大,v(逆)变小 | |
| B. | 恒温恒容,平衡前后混合气体的密度保持不变 | |
| C. | 恒温恒压,充入N2,平衡不移动 | |
| D. | 恒温恒容,充入O2,O2的转化率升高 |
分析 A.升高温度,正、逆速率都增大;
B.混合气体总质量不变,容器容积不变,则容器内混合气体密度始终不变;
C.恒温恒压,充入N2,容器的容积增大,反应混合气体的分压减小,反应向气体分子数目增大的方向移动;
D.增大某一反应物的浓度,平衡正向移动,其它反应物转化率增大,自身的转化率会降低.
解答 解:A.升高温度,正、逆速率都增大,正反应为放热反应,平衡逆向移动,逆反应速率比正反应速率增大的多,故A错误;
B.混合气体总质量不变,恒温恒容条件下容器容积不变,则容器内混合气体密度始终不变,故B正确;
C.恒温恒压,充入N2,容器的容积增大,反应混合气体的分压减小,反应向气体分子数目增大的方向移动,即平衡向逆反应方向移动,故C错误;
D.增大氧气的浓度,平衡正向移动,二氧化硫的转化率增大,氧气的转化率减小,故D错误.
故选:B.
点评 本题考查化学平衡影响因素,理解平衡移动的本质是改变条件导致正逆速率变化不同,C中可以借助浓度不变或平衡常数进行理解.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 | |
| B. | 用醋酸溶液做导电性实验,灯泡很暗 | |
| C. | 0.1mol/L醋酸溶液可以使紫色石蕊试液变红 | |
| D. | 0.1 mol/L醋酸溶液的pH=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
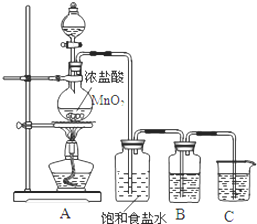 为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3是碱 | B. | NaHCO3是正盐 | C. | NaHCO3是强酸盐 | D. | NaHCO3是酸式盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
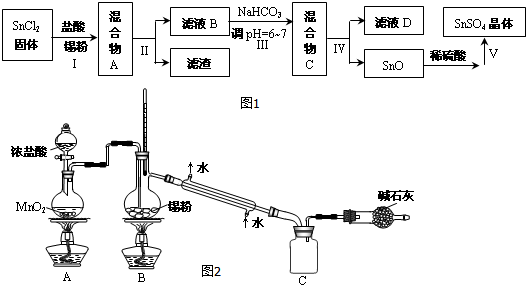
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
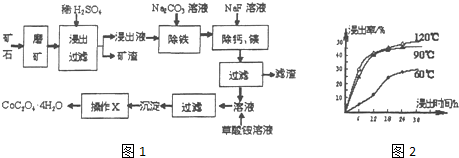
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com