
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 2.8g[CH2 CH2]n 中含有的碳原子数为0.2NA | |
| C. | 1mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |
分析 A.标准状况下,四氯化碳不是气体;
B.[CH2 CH2]n 的最简式为CH2,计算2.8g[CH2 CH2]n 含CH2的物质的量,即可得到含有的碳原子的数目;
C.苯中不含有C=C;
D.乙烷和丙烯含有的氢原子数目相等.
解答 解:A.标准状况下,四氯化碳不是气体,无法进行计算,故A错误;
B.[CH2 CH2]n 的最简式为CH2,2.8g[CH2 CH2]n 含CH2的物质的量为$\frac{2.8}{14}$=0.2mol,故含有的碳原子数为0.2NA,故B正确;
C.苯中不含有C=C,故C错误;
D.乙烷的分子式为C2H6,丙烯的分子式为C3H6,含有的氢原子数目相等,则乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O,故D正确.
故选BD.
点评 本题考查较为综合,侧重于有机物的结构和气体摩尔体积的考查,为高频考点,难度不大.注意相关基础知识的积累.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
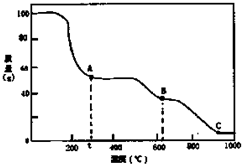
| A. | 0℃→t℃的过程变化是物理变化 | |
| B. | C点物质是工业上冶炼铝的原料 | |
| C. | A→B反应中生成物只有Al2(SO4)3和NH3两种 | |
| D. | Al2(SO4)3能够净水,其原理为:Al3++3OH?Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳的电子式 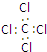 | B. | 乙炔的最简式 CH≡CH | ||
| C. | 聚乙烯的结构简式为 CH2=CH2 | D. | 丙烷的分子结构模型示意图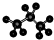 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
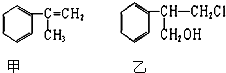
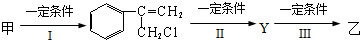
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
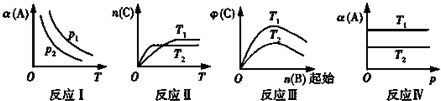
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①②③ | C. | ③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com