
【题目】根据下图所示的反应路线及所给信息填空。

(1)A的名称是____________________![]() 中官能团名称是______________。
中官能团名称是______________。
(2)的反应类型是________________。
(3)反应④的化学方程式是_______________________________。
【答案】环己烷 氯原子 消去反应 ![]() + 2NaOH
+ 2NaOH ![]()
![]() + 2NaBr + 2H2O
+ 2NaBr + 2H2O
【解析】
由合成路线可知,反应①为光照条件下的取代反应,所以A为![]() ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为![]() ,反应④为卤代烃的消去反应生成1,3-环己二烯,据此解答。
,反应④为卤代烃的消去反应生成1,3-环己二烯,据此解答。
(1)由合成路线可知,反应①为光照条件下的取代反应,所以A为![]() ,名称是环己烷,
,名称是环己烷,![]() 的官能团为氯原子,故答案为:环己烷;氯原子。
的官能团为氯原子,故答案为:环己烷;氯原子。
(2)反应②为卤代烃发生的消去反应,故答案为:消去反应。
(3)反应④为![]() 发生消去反应生成1,3-环己二烯,反应方程式为:
发生消去反应生成1,3-环己二烯,反应方程式为:![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,故答案为:
+2NaBr+2H2O,故答案为:![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O。
+2NaBr+2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,则该反应的方程式可表示为()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质G是制备抗癌药物吉非替尼过程中重要的中间体,某研究小组按照下列线路合成中间体G。

已知: 、
、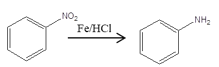 、
、 (同时还有H2O或卤化氢生成)
(同时还有H2O或卤化氢生成)
请回答:
(1)下列说法正确的是_______。
A.化合物A能够使酸性高锰酸钾溶液褪色
B.化合物A中含有4种不同的官能团
C.化合物C具有碱性
D.化合物G的分子式为C15H20N3O3
(2)上述路线中合成A的反应类型为______,化合物E的结构简式为______。
(3)写出C到D的化学反应方程式________。
(4)请设计以乙烯为原料转变为物质C的合成线路(用流程图表示,无机试剂任选)___。
(5)写出化合物B(C8H7NO2)可能的同分异构体_______。须同时满足:①能发生银镜反应;②1H—NMR谱显示分子中含有苯环,且分子中有4种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃经O3氧化后,在锌存在水解可得到醛或酮,现有分子式为C7H14的某烯烃,它与氢气发生加成反应生成2,3-二甲基戊烷,被臭氧氧化后在锌存在下水解生成乙醛和一种酮(![]() ):
):
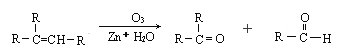
由此可推断该有机物的结构简式为( )
A. ![]() B.
B. 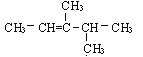
C. ![]() D. (CH3)2C=C(CH3)CH2CH3
D. (CH3)2C=C(CH3)CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用如图所示的装置,进行CO还原Fe2O3的实验(固定装置略)。
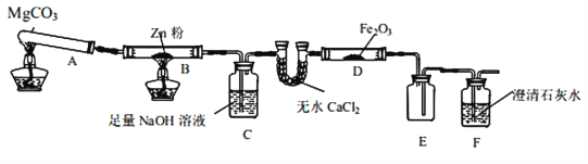
(1)装置B中发生的化学方程式________________。装置C的作用是__________________________
(2)用酒精喷灯对装置D加热,得到灰黑色粉末用黑色粉末进行以下实验:
步骤 | 操作 | 现象 |
1 | 取灰黑色粉末加入稀硫酸 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加NaOH溶液后,在空气中,搅拌放置 | 白色沉淀最终变为红褐色 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水至过量 | 先变红,后褪色 |
①得到的灰黑色粉末是________________(填写化学式)。
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为_________________。
③步骤4中,溶液变红的原因为_____________________________________________________________;溶液褪色可能的原因______________________________________;验证上述原因的实验操作方法为____________。
(3)上述装置,从实验安全考虑,需要采取的改进措施是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA
B. 标准状况下,18g冰水中共价键的数目为NA
C. 56g铁与71gCl2充分反应,转移电子数目为3NA
D. 7.8gNa2O2与足量的水(H218O)反应生成的氧气所含的中子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可用已知浓度的标准I2溶液进行滴定(弱酸性性环境)。该反应的化学方程式为:C6H8O6+I2 = C6H6O6+2HI具体测定步骤及测得数据如下:取10 mL 6 mol·L-1CH3COOH溶液,加入100 mL蒸馏水,将溶液加热煮沸后冷却。精确称取0.2000 g样品,溶解于上述冷却的溶液中,加入1mL指示剂,立即用浓度为0.0500 mol·L-1的标准I2溶液进行滴定到终点,消耗21.00 mL I2溶液。
(1)实验中的指示剂是____________确定达到滴定终点的现象是_____________。
(2)盛装标准I2溶液的是_________(酸式或碱式)滴定管,若滴定结束时俯视滴定管读数(其它操作正确)则滴定结果_______(偏高、偏低或无影响)。
(3)加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用,其目的是_____________。
(4)计算样品中维生素C的质量分数____________(要求列式,且式中各物理量带单位)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com