
| A、核内有8个中子的碳原子:8C |
| B、CS2的结构式:S-C-S |
C、乙烯的比例模型: |
D、NH4Br的电子式: |
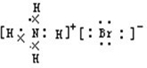 ,故D错误;
,故D错误;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、
| ||||
B、Ag+、H+
| ||||
| C、NH4+、Br-、Na+、SO42- | ||||
D、H+、CI-、Fe2+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.81 g |
| B、5.60 g |
| C、6.20 g |
| D、8.14 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、H+、ClO-、SO32- |
| B、K+、Al3+、Cl-、CO32- |
| C、Na+、Ca2+、HCO3-、OH- |
| D、Al3+、NH4+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压,30g NO气体的分子数为NA |
| B、常温常压下,1mol氦气含有的核外电子数为4NA |
| C、标准状况下,NA个H2O分子所占的体积约为22.4 L |
| D、1mol羟基中电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| 实验 编号 |
T(℃) | NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com