
(7分)(1)实验测得:在室温下1L水中只有10-7mol的水电离,列式计算水的电离平衡常数KH2O;
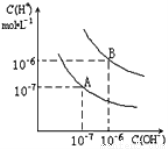
(2)已知水在25℃和100℃时,其电离平衡曲线如图所示,则25℃时水的电离平衡曲线应为_____(填“A”或“B”),请说明理由 。
(7分)(1)1.8×10-16(4分)列式2分 结论2分
(2) A (1分) 原因 温度升高促进水的电离 Kw增大
【解析】
试题分析:(1)1L水的质量是1000g,物质的量是1000g/18g/mol=55.6mol,c(H2O)=55.6mol/L,在室温下1L水中只有10-7mol的水电离,则c(OH-)= c(H+)=1×10-7mol/L,所以KH2O= c(OH-)×c(H+)/ c(H2O)=1×10-14/55.6=1.8×10-16;
(2)水的电离是吸热反应,温度越高,水电离平衡正向移动, c(OH-)、 c(H+)增大,Kw增大 ,
所以25℃时水的电离平衡曲线应为A。
考点:考查对水电离常数的计算,温度对水电离平衡的影响


科目:高中化学 来源:2014-2015安徽省高二上学期第一次质量检测化学试卷(解析版) 题型:填空题
(6分)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高二上学期期中化学试卷(解析版) 题型:选择题
对于可逆反应:2SO2(g)+O2(g) 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
A.增大压强 B.升高温度 C.使用催化剂 D.多充入O2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高一上学期期中化学试卷(解析版) 题型:选择题
下列不属于置换反应的是
A.CuO+H2  Cu+H2O B.C+2CuO
Cu+H2O B.C+2CuO 2Cu+CO2
2Cu+CO2
C.Fe2O3+3CO2 Fe+CO2 D.Fe+CuSO=FeSO+Cu
Fe+CO2 D.Fe+CuSO=FeSO+Cu
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高一上学期期中化学试卷(解析版) 题型:选择题
下列操作中不正确的是
A.过滤时,玻璃棒与三层滤纸的一边接触
B.过滤时,漏斗下端紧贴烧杯内壁
C.加热试管内物质时,试管底部与酒精灯外焰接触
D.向试管中滴加液体时,胶头滴管紧贴试管内壁
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
如果25 ℃时,Kw=1.0×10-14,某温度下Kw=1.0×10-12。这说明
A.某温度下的电离常数较大
B.前者的c(H+)较后者大
C.水的电离过程是一个放热过程
D.Kw和K电离无直接关系
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错误的是

A.a为电池的正极
B.电池充电反应为LiMn2O4===Li1-xMn2O4+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
Li?Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为2Li++FeS+2e-===Li2S+Fe有关该电池的下列说法中,正确的是
A.Li?Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的总反应式为2Li+FeS===Li2S+Fe
C.负极的电极反应式为Al-3e-===Al3+
D.充电时,阴极发生的电极反应式为Li2S+Fe-2e-===2Li++FeS
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江安达市高二第一次月考试卷化学试卷(解析版) 题型:填空题
(11分)测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示.

(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): ;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②若上述实验所测中和热数值偏小,产生偏差的原因可能是( )
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com