
| A. | 自发反应都是放热反应 | |
| B. | 自发反应都是熵增大的反应 | |
| C. | 能自发进行的吸热反应一定是熵增大的反应 | |
| D. | 焓变大于0而熵变小于0的反应肯定自发 |
分析 化学反应是否能自发进行,取决于焓变和熵变,根据△G=△H-T•△S,如△G<0,则反应能自发进行.
解答 解:A、放热反应△H<0,高温下熵变减小的反应,可能△H-T△S>0,放热反应不都是自发反应,故A错误;
B、△S为正值的吸热反应在低温下可能是非自发进行的反应,所以反应不都是自发反应,故B错误;
C、能自发进行的吸热反应△H>0,一定是熵增大的反应,满足△G=△H-T•△S<0,故C正确;
D、焓变大于0而熵变小于0的反应,△H>0,△S<0,△G=△H-T•△S>0,反应一定不能自发进行,故D错误;
故选C.
点评 本题考查了反应自发进行的判断依据和反应焓变熵变的分析应用,反应自发进行是由焓变、熵变、温度共同影响,题目较简单.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol/L | B. | 0.25 mol/L | C. | 0.1 mol/L | D. | 0.225 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56 g CO和32 g O2所具有的总能量小于88 g CO2所具有的总能量 | |
| B. | 碳的燃烧热是△H3 | |
| C. | △H1<△H3 | |
| D. | 28 g CO的总能量比44 g CO2的总能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(1s) | C. | E(4f)<E(4s)<E(3d) | D. | E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ | |
| B. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | |
| C. | 光照氯水有气泡冒出,该气体为Cl2 | |
| D. | 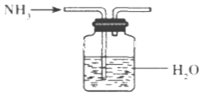 实验室可用如图所示装置制取饱和氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
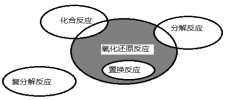 氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )| A. | CuSO4+Mg=Cu+MgSO4 | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | ||
| C. | 2Na2O2+2CO2═2Na2CO3+O2 | D. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Na+、SO42-、Cu2+ | B. | Na+、NH4+、H+、CO32- | ||
| C. | K+、Fe2+、H+、NO3- | D. | Ca2+、Ba2+、SO42-、C1- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com