
【题目】某500 mL溶液中含01 mol Fe2+、02 mol Fe3+,加入02 mol铁粉,待Fe3+ 完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)
A. 04 mol / L B. 0.6 mol / L C. 0.8 mol / L D. 1.0 mol / L
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】下列各组微粒具有相同的电子数的是( )
A.Ar、H2O2 和 C2H6B.CH4、Na+和 K+
C.SiH4、Al3+ 和 Ca2+D.OH﹣,S2﹣ 和 NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子.X与Y形成的化合物的晶胞如图所示,下列关于该晶体的说法正确的是( )
A.1个晶胞中离子的总数为18
B.X2+离子的配位数为8,Y2﹣离子的配位数为4
C.与每个X2+距离最近的X2+共有12个
D.该化合物的化学式为CaS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法正确的是( ) 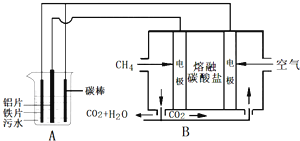
A.装置A中碳棒为阴极
B.装置B中通入空气的电极反应是O2+2H2O+4e-═4OH-
C.污水中加入适量的硫酸钠,既可增强溶液的导电性,又可增强凝聚净化的效果
D.标准状况下,若A装置中产生44.8L气体,则理论上B装置中要消耗CH4 11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl)=1.8×10﹣10 , Ksp(AgI)=1.5×10﹣16 , Ksp(AgBr)=7.7×10﹣13 , 则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>AgBr
B.AgCl>AgBr>AgI
C.AgBr>AgCl>AgI
D.AgBr>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。 
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的。 a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向极(填:“正”或“负”或“阴”或“阳”)。
(3)电解池阳极发生了两个电极反应,电极反应式是 Ⅰ. Fe-2e-=Fe2+ Ⅱ.。
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。 ①负极的电极反应是;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 能电离出H+的化合物叫做酸
B. 氧化还原反应中,得电子越多,氧化性越强
C. 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况
D. 氢氧化钡在水溶液中的电离方程式为:Ba(OH)2=Ba2++2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com