
科目:高中化学 来源:不详 题型:填空题
 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(n+0.2) mol | B.(n+0.4) mol | C.0.28 mol | D.0.31 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
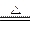 Cu+CO2 ②MgO+2HCl====MgCl2+H2O
Cu+CO2 ②MgO+2HCl====MgCl2+H2O CO2+2H2O
CO2+2H2O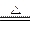 NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O 换反应的有_____________。
换反应的有_____________。 属于复分解反应的有_____________。
属于复分解反应的有_____________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 程式如下:
程式如下: 5Cl 2↑+8H2O
5Cl 2↑+8H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.框图中的物质分别 为:Na2S4O6、H2O、Na2S2O3、Au2O、NaOH 为:Na2S4O6、H2O、Na2S2O3、Au2O、NaOH |
| B.框图中的物质分别为:Na2S2O3、NaOH、Na2S4O6、Au2O、H2O |
| C.框图中的物质分别为:Na2S2O3、H2O、Na2S4O6、Au2O、NaOH |
| D.当1 mol Au2O3完全反应时,转移电子的物质的量为6 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 O
O 离子可与R
离子可与R 离子作用,R
离子作用,R 被氧化为R单质,M
被氧化为R单质,M O
O 的还原产物中,M为+3价;又如c(M
的还原产物中,M为+3价;又如c(M O
O )="0.3" mol·L
)="0.3" mol·L 的溶液100 mL可与c(R
的溶液100 mL可与c(R )="0.6" mol·L
)="0.6" mol·L 的溶液150 mL恰好完全反应,则n值为
的溶液150 mL恰好完全反应,则n值为| A.4 | B.5 | C.6 | D.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com