
【题目】下列关于碳酸钠和碳酸氢钠的比较不正确的是( )
A.二者在水中的溶解度不同,相同温度下,碳酸氢钠的溶解度小于碳酸钠
B.二者热稳定性不同,碳酸钠的热稳定性强于碳酸氢钠
C.二者都能与盐酸反应放出二氧化碳气体,碳酸氢钠俗称苏打或纯碱
D.二者在一定条件下可以相互转化
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】沉淀转化广泛应用于工业生产和科学实验。为了探究AgCl、Ag2S(黑色)的溶解性及转化等相关性质,做以下实验:
步 骤 | 现 象 |
Ⅰ.将NaCl溶液滴入AgNO3溶液中至恰好完全反应。 | 产生白色沉淀。 |
Ⅱ.过滤出Ⅰ中的白色沉淀置于试管中,在试管中加入过量Na2S溶液并充分振荡。 | 白色沉淀变为黑色。 |
Ⅲ.过滤出Ⅱ中的黑色沉淀置于试管中,在试管中加入过量的NaCl溶液并充分振荡后静置。 | 沉淀由黑色最后完全变为乳白色。 |
回答下列问题:
(1)Ⅰ中的白色沉淀是__________。
(2)写出Ⅱ中沉淀变黑的离子方程式__________ ,沉淀转化的主要原因是______________。
(3)滤出步骤Ⅲ中的乳白色沉淀,加入过量的浓HNO3使之充分反应,有红棕色气体生成,尚有部分沉淀未溶解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀;
ⅱ.将Y与足量的KI溶液充分混合,白色沉淀最终转化为黄色沉淀。
① 由ⅰ判断,滤液X中被检出的离子是_______。
② 由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有__________和__________。
(4)为了证明实验步骤Ⅲ中的黑色沉淀只有在NaCl存在下,才能和氧气反应转化为乳白色沉淀,设计了如下对照实验并将实验结果记录在右侧的表格中。
装置 | 实验结果 |
B | 一段时间后,出现乳白色沉淀 |
C | 一段时间后,无明显变化 |
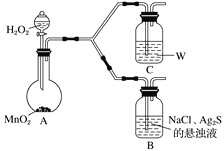
①A中,盛有MnO2的玻璃仪器名称是_________________。
②C中盛放的是物质W的悬浊液,W是________(填化学式)。
③请完成B中发生反应的反应式并配平:_____
Ag2S+ + + H2O![]() AgCl+ + NaOH
AgCl+ + NaOH
________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。

已知:在溶液中,FeSO4+NO![]() [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列对该实验相关描述错误的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列对该实验相关描述错误的是
A. 装置F、I中的试剂依次为水,硫酸亚铁溶液
B. 装置J收集的气体中不含NO
C. 实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D. 若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,对于该溶液,下列叙述中正确的是
A. 水电离出来的c(H+)=1×10-10mo1·L-1
B. 此时水的离子积KW=1×10-4
C. c(H+)=2[c(OH-)+c(SO42-)]
D. 该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
A.硫酸、CuSO45H2O,苛性钾
B.硫酸、空气、纯碱
C.氧化铁、胆矾、熟石灰
D.硝酸、食盐水、烧碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂。

下列关于实验现象的解释或结论正确的是
选项 | 实验现象 | 解释或结论 |
A | a中无明显现象 | Na2SO3和H2O2一定不发生反应 |
B | b中加稀H2SO4后才产生淡黄色沉淀 | SO32和S2两种离子一定不能大量共存 |
C | c中加BaCl2溶液后产生白色沉淀且红色褪去 | Ba2++ SO32 == BaSO3↓,使SO32水解平衡逆向移动,红色褪去 |
D | d中产生白色沉淀 | 原Na2SO3溶液中含有SO42 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国芒硝(Na2SO4·10H2O)的储量丰富,它是重要的化工原料。
(1)制备碳酸钠。
①以芒硝和碳酸氢铵为原料,在水溶液中经复分解反应析出NaHCO3晶体,其反应的化学方程式是________。
②已知:ⅰ.2NaOH(s) + CO2(g) == Na2CO3(s) + H2O(g) ΔH1=127.4 kJ·mol 1
ⅱ.NaOH(s) + CO2(g) == NaHCO3(s) ΔH2=131.5 kJ·mol 1
反应2NaHCO3(s) == Na2CO3(s) + H2O(g) + CO2(g) ΔH= ________ kJ·mol 1。
(2)制备烧碱和硫酸。
用右图所示装置,以惰性电极进行电解,ab、cd均为离子交换膜。则阳极区制备的溶液是________,阴极的电极反应式是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是应用非常广泛的有机溶剂,主要用于涂料、油墨、粘合剂、胶片、医药、化工、电子、化妆品及食品行业等。实验室可用乙酸与乙醇反应制备乙酸乙酯。
(1)为判断乙酸乙酯中与乙基(-CH2CH3)相连的氧原子的来源,请没计一种可进行判别的方案__________。(无需给出实验装置实验步骤,只需给出设计思想)。
(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用下图所示装置进行以下四个实验,实验结束后充分振荡试管II再测有机层的厚度,实验记录如下:
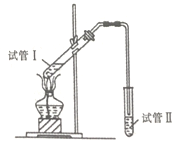
编号 | 试管I中的试剂 | 有机层厚度/cm |
A | 3mL乙醇、2mL乙酸、1mL18mol/L浓硫酸 | 3.0 |
B | 3mL乙醇、2mL乙酸 | 0.1 |
C | 3mL乙醇、2mL乙酸、6mL3mol/L硫酸 | 1.2 |
D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①试管II中试剂的名称为_______,其作用是__________。
②分析比较实验_____(填实验编号)的数据,可推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
③分析比较实验C、D,证明对酯化反应具有催化作用的是H+。实验D中应加入盐酸的体积和浓度分别是_______mL和_____mol/L。
(3)现代化工生产探索以CH3CHO为原料,用(CH3CH2O)3Al作催化剂,合成乙酸乙酯:2CH3CHO![]() CH3COOCH2CH3
CH3COOCH2CH3
在实验室中进行该实验时,不同条件下的实验结果如下表所示:
实验序号 | 催化剂用量/g | 反应温度/℃ | 反应时间/h | 副产物/% | 选择性/% | 转化率/% |
1 | 0.368 | 6.5-2 | 52 | 0.35 | 99.9 | 99.6 |
2 | 0.278 | 10-0.5 | 52 | 0.12 | 99.81 | 95.39 |
3 | 0.368 | 6.5-2 | 12 | 0.1 | 99.8 | 99.7 |
4 | 0.368 | 10-0.5 | 52 | 0.8 | 99.5 | 97.3 |
(注)选择性:转化的CH3CHO中生成CH3COOCH2CH3的百分比。
下列说法正确的是_______(填编号)。
A.用乙醛合成乙酸乙酯,可减少“工业三废”的排放
B.温度越高反应速率越快,乙醛的转化率越高
C.用乙醛合成乙酸乙酯的反应时间控制在12h为宜
D.催化剂用量不会影响合成反应的选择性转化率
E.(CH3CH2O)3Al是乙醛制乙酸乙酯的高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是一种重要的非金属单质,硅及其化合物的用途非常广泛。根据所学知识回答硅及其化合物的相关问题。
(1)硅的最高价氧化物对应水化物化学式可能是_____。
A.H4SiO3 B.H2SiO3 C.H3SiO4 D.HSiO4
(2)金刚石与金刚砂(SiC)具有相似的晶体结构,在金刚砂的空间网状结构中,碳原子、硅原子交替以共价 单键相结合。金刚砂属于_____晶体。金刚砂的熔点比金刚石的熔点_____;金刚砂的结构中,一个硅原子周围结合_____个碳原子。
(3)晶体硅的微观结构与金刚石相似,晶体硅中 Si—Si 键之间的夹角大小约为_____。 下表列有三种物质(晶体)的熔点:
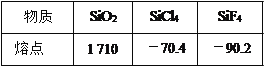
简要解释熔点产生差异的原因:
①SiO2 和 SiCl4:_________________________;
②SiCl4和 SiF4:___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com