
|
浓硫酸的性质有:①酸性、②强氧化性、③脱水性、④难挥发性等.乙醇、溴化钠和浓硫酸混合共热制备溴乙烷时,会有多个副反应发生,此过程中浓硫酸显示的性质是 | |
| [ ] | |
A. |
①②③④ |
B. |
①和② |
C. |
只有① |
D. |
①和④ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
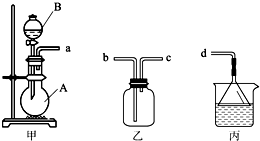 液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:
液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
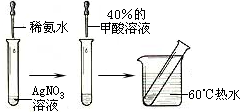 (2009?汕头二模)甲酸(CH2O2),俗称蚁酸,结构式为:
(2009?汕头二模)甲酸(CH2O2),俗称蚁酸,结构式为: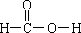
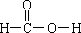



查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
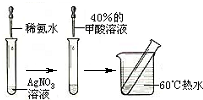 甲酸(CH2O2),俗称蚁酸,结构式为:
甲酸(CH2O2),俗称蚁酸,结构式为:| 水浴 |
| 水浴 |
查看答案和解析>>
科目:高中化学 来源: 题型:
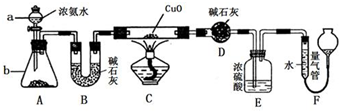 某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题:
某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如图实验(夹持装置未画出)进行实验.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com