
【题目】具有下列电子排布式的原子中,半径最大的是( )
A. 1s22s22p63s1B. 1s22s22p2C. 1s22s22p3D. 1s22s22p63s2
科目:高中化学 来源: 题型:
【题目】下列有关材料的说法错误的是( )
A. 铝制品表面有一层致密的氧化膜 B. 二氧化硅常用于制造光导纤维
C. 实验室中经过滤可得到纳米碳酸钙固体 D. 聚乙烯可作食品包装材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则参加反应的Cr3+与PbO2的物质的量之比为
A. 1:l B. 2:3 C. 3:2 D. 4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验.测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度.
实验原理:2Na2CO4+4HCl═4NaCl+2CO2↑+O2↑+2H2O
实验装置:
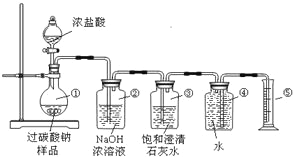
交流与讨论:
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品的纯度.
(1)装置②的作用是_________________。
(2)装置③的作用是:__________________。
(3)称取适量样品与足量浓盐酸充分反应后,收集到的氧气的体积为0.25L(已知该实验条件下氧气的密度为1.28g/L),则称取的样品质量应大于_______________g。
Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度.但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是_________________;(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g.则该样品的纯度为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A. 1L 0.1 molL-1的氨水中有0.1![]() 个NH4+
个NH4+
B. 标准况下,22.4L盐酸含有![]() 个HCl分子
个HCl分子
C. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为0.5 ![]()
D. 标准状况下,6.72 LN02与水充分反应转移的电子数目为0.2 ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com