
下列叙述正确的是
| A.用湿润的pH试纸测溶液的pH |
| B.用蒸馏法可将海水淡化为可饮用水 |
| C.常温下浓硫酸不能盛放在铝制容器中 |
| D.配制溶液时仰视容量瓶刻度线定容会使溶液浓度偏高 |
科目:高中化学 来源: 题型:单选题
下列装置和操作能达到实验目的的是( )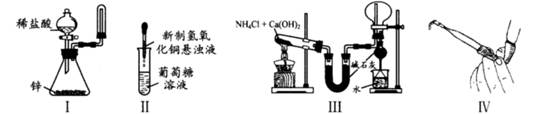
| A.实验I:制取并收集氢气 |
| B.实验II:验证葡萄糖的还原性 |
| C.实验III:实验室制氨气并收集干燥的氨气 |
| D.实验Ⅳ:检查碱式滴定管是否漏液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为测定碳酸氢钠纯度(含有少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
| A.可用稀盐酸代替稀硫酸 |
| B.量气管中液体为水 |
| C.反应完全后,冷却,读取量气管体积数,再减去所加硫酸的体积,即为生成的气体体积 |
| D.实验测得该试样中碳酸氢钠质量分数偏高,可能是测定气体体积时未冷却至室温 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列根据实验操作和现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 测定等浓度的Na2CO3和Na2SO3 溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| B | SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | SO2具有漂白性 |
| C | 溴乙烷与NaOH溶液共热后,加HNO3酸化的AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| D | 向等浓度的KBr、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgBr)> Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某同学在实验报告中记录下列数据,其中正确的是( )
| A.用25mL量筒量取12.36mL盐酸 |
| B.用托盘天平称取8.75g食盐 |
| C.用酸式滴定管量取23.22mL高锰酸钾溶液 |
| D.用广泛pH试纸测得某溶液pH为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3 + S  Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Ⅰ.现按如下方法制备Na2S2O3·5H2O:
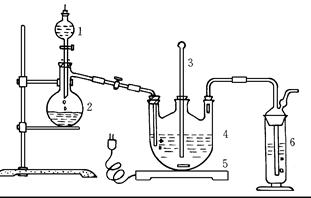
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按下图安装好装置。
(1)仪器2的名称为 ,
装置6中可放入 。
| A.BaCl2溶液 | B.浓H2SO4 | C.酸性KMnO4溶液 | D.NaOH溶液 |
 Na2S2O3
Na2S2O3
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学实验的描述中正确的是
| A.分离乙醇和乙酸要用分液的方法 |
| B.配制一定物质的量浓度的NaCl溶液,如果NaCl固体中含有Na2CO3,所配制溶液中c(Na+)将偏高 |
| C.某无色溶液中加稀硫酸产生无色无味气体,该气体能使澄清石灰水变浑浊,说明该溶液中含CO32- |
D.平衡2NO2 N2O4(无色),减压时,气体颜色变浅,平衡向正反应方向移动 N2O4(无色),减压时,气体颜色变浅,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列根据实验及现象得出的结论不正确的是
| | 实 验 | 现 象 | 结论 | ||
| A |  液体X | 试管(1)中紫色消失,试管(2)中紫色没有消失 | 甲苯中苯环使甲基的活性增强 | ||
| B |
   | 试管内壁有 银镜生成 | X具有还原性,一定含有醛基 | ||
| C | 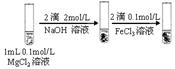 | 先生成白色沉淀,滴加FeCl3溶液后,生成红褐色沉淀 | Fe(OH)3是比Mg(OH)2 更难溶的电解质 | ||
| D |  | 试管b 比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com