
科目:高中化学 来源:不详 题型:填空题
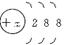
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
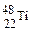 和
和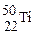 的说法中正确的是
的说法中正确的是 A.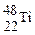 和 和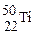 的质量数相同,互称为同位素 的质量数相同,互称为同位素 |
B.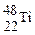 和 和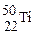 的质子数相同,互称同位素 的质子数相同,互称同位素 |
C.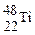 和 和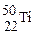 的质子数相同,是同一种核素 的质子数相同,是同一种核素 |
D.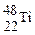 与 与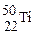 核外电子数相同,中子数不同,不能互称为同位素 核外电子数相同,中子数不同,不能互称为同位素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
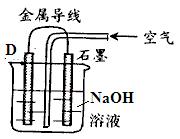
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲认为上述发现绝对不可能,因为H3的分子违背了价键理论 |
| B.乙认为宇宙中还存在另一种氢单质,因为氢有三种同位素,必有三种同素异形体 |
| C.丙认为如果上述发现存在,则证明传统价键理论的局限性而有待发展 |
D.丁认为H3分子实质上是H2分子与H+以配位键结合的产物,应该写成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③④⑤⑦⑧⑨ | B.③⑥⑦⑧ |
| C.③⑥⑦⑧⑨ | D.①②③④⑤⑥⑦⑧⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com