
【题目】I、300℃时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)2Z(g)ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
(1)反应0~2minZ的平均速率v(Z)=____
(2)能判断该反应已经达到平衡状态的是____
A.生成X的速率是生成Z的速率的2倍 B.容器内压强保持不变
C.容器内气体的密度保持不变 D.容器内各气体的浓度保持不变
(3)温度为300℃时,该反应的化学平衡常数K= ___
II、(1)常温下,0.005mol·L-1Ba(OH)2溶液的pH=_____
(2)常温下,向0.1mol·L-1NH3·H2O溶液中不断加水,过程中c(OH-)/c(NH3·H2O)将____(选填“增大”、“减小”或“不变”)
(3)下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)
Fe3+ | Al3+ | Zn2+ | |
开始沉淀的pH | 1.1 | 3.2 | 5.9 |
完全沉淀的pH | 3.2 | 5 | 8.9 |
某溶液中含Fe3+、Al3+、Zn2+,欲除去Fe3+、Al3+,向其中滴加1.0moL·L-1的NaOH溶液调节溶液的pH为___。
【答案】0.004mol·L-1·min-1 D 1.44 12 增大 5~5.9或其间的一个值
【解析】
I.(1)2min内Y物质的量变化为0.16mol-0.12mol=0.04mol,根据v=![]() 计算v(Y),再利用速率之比等于化学计量数之比计算v(Z);
计算v(Y),再利用速率之比等于化学计量数之比计算v(Z);
(2)结合平衡状态的特征判断即可;
(3) 由表中数据可知7min时,反应到达平衡,根据平衡时Y的物质的量,计算平衡时其它组分的物质的量,由于反应气体氢气的化学计量数相等,用物质的量代替浓度代入平衡常数表达式K=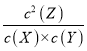 计算;
计算;
II.(1) 常温下,Kw=1×10-14,0.005mol·L-1Ba(OH)2溶液中c(OH-)=0.01 mol·L-1,c(H+)=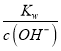 ;
;
(2)向0.1mol·L-1NH3·H2O溶液中不断加水,促进NH3·H2O的电离,溶液中c(OH-)和c(NH3·H2O)均减小,但n(OH-)的数目增多,而n(NH3·H2O)数目减小;
(3) 根据表中数据分析Fe3+、Al3+沉淀完全时溶液的pH,Zn2+开始沉淀时的pH,确定调节溶液的pH范围。
I.(1) 2min内Y物质的量变化为0.16mol-0.12mol=0.04mol,则v(Y)= =0.002mol/(Lmin),速率之比等于化学计量数之比,v(Z)=2v(Y)=0.004 mol/(Lmin);
=0.002mol/(Lmin),速率之比等于化学计量数之比,v(Z)=2v(Y)=0.004 mol/(Lmin);
(2) A.生成Z的速率(为正反应)是生成X的速率(为逆反应)的2倍,反应达到平衡状态,而题给信息,速率之比不等于系数比,反应没有达到平衡状态,故A错误;
B.恒温恒容下,反应前后气体物质的量不变,容器内压强始终保持不变,故B错误;
C.混合气体总质量不变,容器容积不变,容器内气体的密度始终保持不变,故C错误;
D.容器内各气体的浓度保持不变,说明反应到达平衡,故D正确;
故答案为D;
(3) 由表中数据可知7min时,反应到达平衡,平衡时Y的物质的量为0.1mol,则:
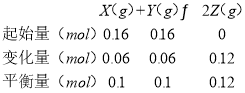
由于反应前后气体的化学计量数相等,用物质的量代替浓度计算,平衡常数K=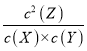 =
=![]() =1.44;
=1.44;
II、(1) 常温下,Kw=1×10-14,0.005mol·L-1Ba(OH)2溶液中c(OH-)=0.01 mol·L-1,c(H+)=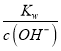 =1×10-12 mol·L-1,则溶液的pH=12;
=1×10-12 mol·L-1,则溶液的pH=12;
(2) 向0.1mol·L-1NH3·H2O溶液中不断加水,促进NH3·H2O的电离,溶液中c(OH-)和c(NH3·H2O)均减小,但n(OH-)的数目增多,而n(NH3·H2O)数目减小,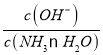 =
=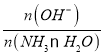 ,则
,则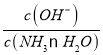 将随水量的增加而增大;
将随水量的增加而增大;
(3) Fe3+沉淀完全时溶液的pH为3.2、Al3+沉淀完全时溶液的pH为5,而Zn2+开始沉淀时的pH为5.9,则欲除去Fe3+、Al3+,调节溶液的pH范围为5~5.9。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】铅的单质、氧化物、盐在现代工业中有着重要用途。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为_______。
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
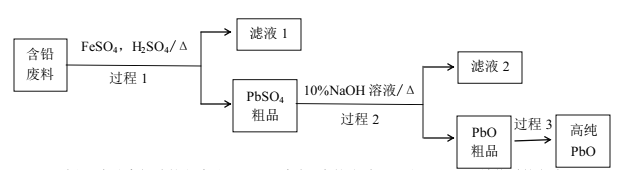
过程1中分离提纯的方法是___,滤液2中的溶质主要是____填物质的名称)。过程1中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是_______。
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
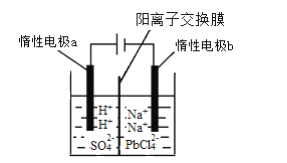
①写出电解时阴极的电极反应式_________。
②电解过程中通过阳离子交换膜的离子主要为____。
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向____极室(填“阴”或者“阳”)加入____(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,下列有关表述错误的是

A.利用了电解原理
B.钢管桩上有刺激性气味气体生成
C.电子由电源负极流向钢管桩
D.高硅铸铁作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若A、B、C三种物质的溶液均显碱性,焰色反应均为黄色,受热分解可转化为B。
①A与过量W转化为C的总反应的离子方程式为__;
②A溶液与C溶液反应的化学方程式为__。
(2)若B的溶液显黄色,一定条件下B的饱和溶液可与沸水反应生成红褐色分散系。
①实验室制A单质的反应的离子方程式为__;
②C溶液中加入氢氧化钠溶液的现象:__;
③一定条件下W与水反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知少量碳酸钠与足量盐酸反应,有二氧化碳气体放出;而少量盐酸与过量碳酸钠反应,则生成碳酸氢钠和氯化钠,无气体放出。现有A、B两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定两瓶溶液的成分及物质的量浓度,进行以下实验:
①取20mLA溶液,向其中缓慢滴入B溶液25mL,共收集到112mL(标准状况)气体。
②取25mLB溶液,向其中缓慢滴入A溶液20mL,共收集到56mL(标准状况)气体。
(1)写出少量盐酸与过量碳酸钠反应,无气体放出的离子方程式______;
(2)为使上述①②反应完全,还需加入______;(填“稀盐酸”或“碳酸钠溶液”)A溶液的物质的量浓度为______mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如CH3CH=CHCH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A. X的化学式为C8H8
B. 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C. X能使酸性高锰酸钾溶液褪色
D. X与足量的H2在一定条件下反应可生成饱和烃Z, Z的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)甲基的电子式为________,0.5 mol甲基中含有_____mol电子。
(2)丙烷的结构简式为________,该物质常温下为______(填“气态”“液态”或“固态”)。
(3)分子中含30个氢原子的烷烃的分子式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______和________。含有12mol σ键的K4[Fe(CN)6的物质的量为________mol。
(3)黄血盐中N原子的杂化方式为______;C、N、O的第一电离能由大到小的排序为_____,电负性由大到小的排序为________。
(4)Fe、Na、K的晶体结构如图所示:
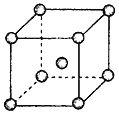
① 钠的熔点比钾更高,原因是__________________________。
② Fe原子半径是r cm,阿伏加德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______g/cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com