
| A. | 化学反应速率是化学反应进行快慢程度的物理量 | |
| B. | 化学反应速率的常用单位有mol/(L•s)和mol/(L•min) | |
| C. | 在同一个反应中,可以用反应物或生成物来表示反应速率 | |
| D. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 |
分析 化学反应速率是表示化学反应进行快慢程度的物理量,为单位时间内浓度的变化,单位为mol/(L•s)和mol/(L•min),同一个化学反应中,可用不同物质表示化学反应速率,反应速率之比等于化学计量数之比,以此解答该题.
解答 解:A.化学反应速率是衡量化学反应进行快慢程度的物理量,反应速率越大,反应越快,故A正确;
B.反应速率单位是导出单位,浓度单位常用mol/L,时间单位常用s、min,化学反应速率的常用单位有mol•L-1•S-1和mol/(L•min),故B正确;
C.在同一个反应中,时间相同体积相同,速率之比等于物质的量之比,而物质的量之比等于化学计量数之比,所以各物质的反应速率之比等于化学方程式中的系数比,故C正确;
D.化学反应速率通常用单位时间内反应物浓度或生成物浓度的变化量表示,故D错误.
故选D.
点评 本题考查了学生对化学反应速率概念的理解,为高频考点,侧重考查学生的分析能力,理解化学反应速率时注意:化学反应速率是平均值不是即时值;化学反应速率没有负值;同一化学反应中,各物质的化学反应速率之比等于其计量数之比;纯固体、液体一般不使用该方法表示反应速率.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | 明矾的主要成分是氢氧化铝 | B. | CH3OH可导致人体中毒 | ||
| C. | SO2可大量用于漂白食品 | D. | Na2CO3可以做胃药 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇不能与NaOH溶液反应,苯酚可以与NaOH溶液反应,说明苯环对羟基产生影响 | |
| B. | 苯不能被酸性KMnO4溶液氧化,甲苯可以被酸性KMnO4溶液氧化为苯甲酸,说明侧链对苯环产生了影响 | |
| C. | 苯与苯酚与溴水反应的条件、产物区别,说明羟基对苯环产生影响 | |
| D. | 苯和甲苯硝化反应产物的区别,说明甲基对苯环产生影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
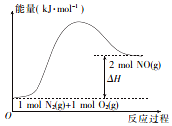 汽车发动机在工作时,由于电喷,在气缸中会发生反应:N2(g)+O2 (g)=2NO(g).已知该反应过程中的能量变化如图所示,下列说法中不正确的是( )
汽车发动机在工作时,由于电喷,在气缸中会发生反应:N2(g)+O2 (g)=2NO(g).已知该反应过程中的能量变化如图所示,下列说法中不正确的是( )| A. | 该反应是放热反应 | |
| B. | 该反应是氧化还原反应 | |
| C. | 该反应过程中有共价键的断裂和形成 | |
| D. | 使用催化剂可以改变反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
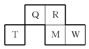 Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )| A. | MW6中各原子核外均满足8电子稳定结构 | |
| B. | Q、W的单核离子的核外电子数相等 | |
| C. | 五种元素均能形成氢化物 | |
| D. | W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
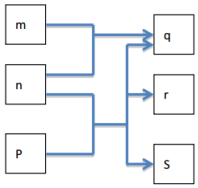 短周期元素W、X、Y、Z分别属于三个周期,其原子序数依次增大,Y的原子半径是短周期主族元素中最大的.由W、X、Y、Z组成的物质之间存在下图所示的转化关系,其中m是元素Y的单质,n是元素Z的单质,通常为黄绿色气体,s的水溶液常用作漂白剂和消毒剂.
短周期元素W、X、Y、Z分别属于三个周期,其原子序数依次增大,Y的原子半径是短周期主族元素中最大的.由W、X、Y、Z组成的物质之间存在下图所示的转化关系,其中m是元素Y的单质,n是元素Z的单质,通常为黄绿色气体,s的水溶液常用作漂白剂和消毒剂. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH+3O2=2CO2+3H2O△H=-1367.0 kJ•mol-1 | |
| B. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3 kmol-1 | |
| C. | S(s)+O2(g)=SO2(g)△H=-269.8 kJ•mol-1 | |
| D. | 2NO(g)+O2(g)=2NO2(g)△H=-116.2 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com