
【题目】过氧化氢(H2O2,氧显-1价)俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。

根据下列反应回答问题:
A.Ag2O+H2O2=2Ag+O2↑+H2O
B.2H2O2=2H2O+O2↑
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2分别表现_______性质。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序____。
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为____。
【答案】A中体现还原性,B中既体现氧化性又体现还原性,C中体现氧化性。 Ag2O>H2O2>K2CrO4 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
【解析】
(1)根据H2O2中氧元素的化合价变化进行分析;
(2)根据氧化剂的氧化性强于氧化产物的氧化性进行分析;
(3)根据得失电子相等、原子守恒和电荷守恒配平;
(1)A中氧的化合价升高,体现还原性,B中双氧水中氧元素化合价既升高也降低,既体现氧化性又体现还原性,C中双氧水中氧元素化合价降低,说明双氧水作氧化剂,体现了氧化性。
答案:A中体现还原性,B中既体现氧化性又体现还原性,C中体现氧化性
(2)反应Ag2O+H2O2====2Ag+O2↑+H2O中,氧化银作氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH====2K2CrO4+3K2SO4+8H2O中,双氧水作氧化剂,铬酸钾作氧化产物,则氧化性H2O2>K2CrO4,故氧化性顺序为Ag2O>H2O2>K2CrO4;
答案:Ag2O>H2O2>K2CrO4
(3)H2O2只发生了H2O2→O2的变化体现了双氧水的还原性,作还原剂,所以高锰酸根作氧化剂,还原产物是锰离子,根据电子守恒、原子守恒和电荷守恒配平离子方程式:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O。
答案: 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有Fe3+、Cu2+、SO42-等离子,为了减少污染并变废为宝,工厂计划从该废水中回收金属铜并得到硫酸亚铁(Fe+2FeCl3=3FeCl2)。生产流程如下图所示(所加试剂均为过量)请回答:

(1)试剂①应该是___________,A 中含有的物质是_________(填物质的名称)。
(2)步骤①采取的操作为__________,步骤③中还需分离提纯方法是蒸发浓缩、______。
(3)写出步骤②中发生的离子方程式:________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯氨铂是一种治疗癌症的常用化学药物,具有较高疗效。其中的金属Pt(铂元素)是原子序数为78(质量数为195)的原子,则Pt的中子数与质子数之差是
A.117B.78C.39D.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0。
N2(g)+2CO2(g) ΔH<0。
(1)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
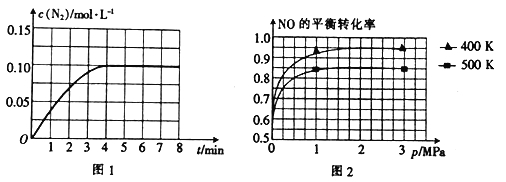
(2)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=_________,4 min末CO的浓度为_____________ molL-1。
(3)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AgCl 的Ksp=1.8×10-10,在100mL1.0×10 -4mol/L 的KCl 溶液中,加入100mL2.0×10-6mol/L的AgNO3 溶液,下列说法正确的是
A. 有AgCl 沉淀生成 B. 无AgCl沉淀生成
C. 有沉淀生成但不是AgCl D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某同学进行CO2 与Na2O2 反应的探究实验,回答下列问题。
(1)用下图装置制备纯净的CO2

①丙装置的名称是__________,乙、丙装置中盛装的试剂分别是__________、_________。
②若CO2 中混有HCl,则HCl 与Na2O2 反应的化学方程式为_____________。
(2)按照下面的装置图进行实验(夹持装置略)。

①先组装仪器,然后_____________,再用注射器1 抽取100 mL 纯净的CO2,将其连接在K1 处,注射器2 的活塞推到底后连接在K2 处,具支U 形管中装入足量的Na2O2 粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1 的活塞,可观察到的现象是_________。
③实验过程中,需缓慢推入CO2,其目的是_____________,为达到相同目的,还可进行的操作是_____________。
(3)实验结束后,当注射器1 的活塞推到底时,测得注射器2 中气体体积为65 mL,则CO2的转化率是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机分子中,所有的原子不可能处在同一平面的是( )
A. CH2=CH-CNB. CH2=CH-CH=CH2
C. 苯乙烯D. 2-甲基-1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成一种用于合成γ分泌调节剂的药物中间体,其合成的关键一步如图。

下列有关化合物A、B的说法正确的是( )
A. A→B的反应为取代反应
B. A分子中所有碳原子一定在同一平面上
C. A、B均不能使酸性KMnO4溶液褪色
D. B与足量H2完全加成的产物分子中含有4个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下

已知:(1) AlCl3·6H2O易溶于水、乙醇及乙醚;
(2) 明矾在水中的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅱ中生成Al(OH)3的离子方程式为____________________________________________。
(2)步骤Ⅲ灼烧Al(OH)3所用实验室常用仪器为________,为了提高Al2O3纯度,需________(填操作步骤)。
(3)制备AlCl3·6H2O的工业生产中,胶状固体用酸浸取后,还需要通入HCl气体。通入HCl的作用主要有两点:____________和____________。
(4)已知:在不同温度条件下向一定量的氯化铝溶液中通入HCl气体,通入量对AlCl3·6H2O结晶量和结晶效率的影响如图,请补充完整由胶状固体制备AlCl3·6H2O晶体的实验方案:向胶状固体滴加一定浓度盐酸,直至恰好完全溶解,__________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com