
 ��
�� ��
������ ��1������n=$\frac{m}{M}$��Ϸ��ӵ���ɷ������
��2������Ħ�������ĸ���������㣬Ħ��������ֵ�ϵ�������Է������������ݻ�ѧʽ����A�����ԭ���������ж�Ԫ�����࣬�ٻ���A2+�Ľṹʾ��ͼ��
��3����ͬ�����£����֮�ȵ������ʵ���֮�ȵ��ڷ�����֮�ȣ��ݴ��жϷ�Ӧ����ʽ�����ʵĻ�ѧ�����������ݷ���ʽԭ���غ����C�Ļ�ѧʽ��
��4�����ڸ÷�Ӧ���̴�+7�۽�Ϊ+2�ۣ��ȴ�-1����Ϊ0�ۣ����ݻ��ϼ����������ԭ���غ����ƽ��
�ڷ�Ӧ���ɱ�������HClȫת��Ϊ����������������������㣮
��� �⣺��1����ͬ���ʵ�����CO2��O2���京�е�O�����ʵ���Ϊ3��2������ԭ����֮��Ϊ3��2���������֮��Ϊ22��16=11��8��������ͬ��CO2��O2�������ʵ���֮��Ϊ $\frac{m}{44}��\frac{m}{32}$=8��11��
�ʴ�Ϊ��3��2��11��8��
��2��19gij���۽������Ȼ���ACl2�к���0.4mol Cl-����ACl2�����ʵ���Ϊ0.2mol��Ħ������=$\frac{19g}{0.2mol}$=95g/mol��ACl2��A�����ԭ������=95-35.5��2=24���������ԭ������Ϊ24��Ϊþ����Mg2+�Ľṹʾ��ͼΪ ��
��
�ʴ�Ϊ��95g/mol�� ��
��
��3������5�������A2��15���������B2��ȫ��������10���ij����C������A2��B2��C�Ļ�ѧ������֮��Ϊ1��3��2�����Է���ʽΪA2+3B2=2C������ԭ���غ��֪C�Ļ�ѧʽΪAB3��B3A��
�ʴ�Ϊ��AB3��B3A��
��4�����ڸ÷�Ӧ���̴�+7�۽�Ϊ+2�ۣ��ȴ�-1����Ϊ0�ۣ���������ԭ��ӦԪ�ػ��ϼ����ߵ������뽵�͵�����Ӧ��ȣ���������غ��֪���÷�Ӧ�ķ���ʽΪ2KMnO4+16HCl�T2MnCl2+2KCl+5Cl2��+8H2O���÷�Ӧת��10e-��˫���ű�����ӵ�ת�Ʒ������ĿΪ ��
��
�ʴ�Ϊ�� ��
��
������4.48L��������״�������ɣ���n��Cl2��=$\frac{4.48L}{22.4L/mol}$=0.2mol����Ӧ���ɱ�������HClȫת��Ϊ��������Cl�غ��֪����������HClΪ0.4mol��
�ʴ�Ϊ��0.4mol��
���� ���⿼�������ʵ����ļ��㡢������ԭ��Ӧ���������ʵ����ļ��㹫ʽ����Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ������ط��������ͼ��������Ŀ��飬�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
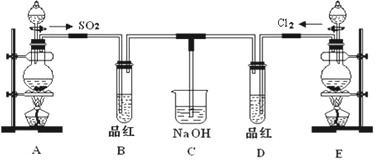
| A�� | ֻ�Т� | B�� | ���� | C�� | �ۢܢ� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ӡˢ��·�壺Fe3++Cu�TFe2++Cu2+ | |
| B�� | Ca��HCO3��2��Һ�м�����NaOH��Һ��HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| C�� | ����þ��Һ������������Һ��Ӧ��SO42-+Ba2+�TBaSO4�� | |
| D�� | KClO3��Һ��Ũ���ᷴӦ��ClO3-+5Cl-+6H+�T3Cl2��+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl-��Br-��I- | B�� | Br-��I-��Cl- | C�� | Br-��Cl-��I- | D�� | Cl-��I-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1 CH3COONa��Һ��0.1 mol•L-1 HCl��Һ�������ϣ�c��Na+��=c��Cl-����c��CH3COO-����c��OH-�� | |
| B�� | 0.1 mol•L-1 NH4Cl��Һ��0.1 mol•L-1��ˮ�������ϣ�pH��7����c��NH3•H2O����c��NH4+����c��Cl-����c��OH-�� | |
| C�� | 0.1 mol•L-1 Na2CO3��Һ��0.1 mol•L-1 NaHCO3��Һ�������ϣ�$\frac{3}{2}$c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 0.1 mol•L-1 Na2C2O4��Һ��0.1 mol•L-1 HCl��Һ�������ϣ�H2C2O4Ϊ��Ԫ���ᣩ��2c��C2O42-��+c��HC2O4-��+c��OH-��=c��Na+��+c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
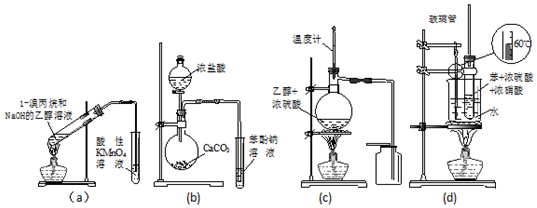
| A�� | aװ��ֱ��������KMnO4��Һ������ȥ��Ӧ�IJ��� | |
| B�� | bװ�ü������ԣ����̼����� | |
| C�� | cװ������ʵ������ȡ���ռ���ϩ | |
| D�� | dװ������ʵ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
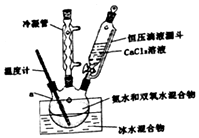 �������ƣ�CaO2����һ�ְ�ɫ�ᾧ���ĩ��������ˮ�������ڴ��ࡢ���ѵȣ�������150�����ҿ�ʼ�ֽ�ų���������ˮ������Ӧ����H2O2�������ᷴӦ����H2O2
�������ƣ�CaO2����һ�ְ�ɫ�ᾧ���ĩ��������ˮ�������ڴ��ࡢ���ѵȣ�������150�����ҿ�ʼ�ֽ�ų���������ˮ������Ӧ����H2O2�������ᷴӦ����H2O2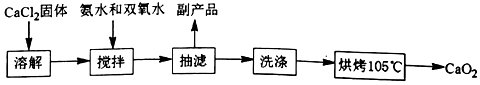
| ���� ʱ�� | ��Ʒȡ������/��g�� | ƽ�����������KMnO4��/mL |
| ����ǰ�ⶨ | a | 25.00 |
| ����һ���º�ⶨ | a | 24.00 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com