
【题目】下列属于电解质并能导电的物质是
A.熔融的NaCl B.KNO3溶液 C.单质铜 D.酒精
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来区别它们的试剂是
A.酚酞试液 B.紫色石蕊试液
C.AgNO3 溶液 D.NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜,当两装置电路中通过的电子都是1mol时,下列说法不正确的是
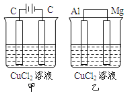
A.溶液的导电能力变化:甲>乙
B.溶液的质量减小程度:甲>乙
C.甲中阴极和乙中镁电极上析出物质质量:甲=乙
D.电极反应式:甲中阳极:2Cl--2e-=Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molH2(g)和2molI2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g)![]() 2HI(g)△H<0,并达到平衡。HI的体积分数w(HI)随时间变化如下图(Ⅱ)所示,若改变反应条件,w(HI)的变化曲线如下图(Ⅰ)所示,则改变的条件可能是
2HI(g)△H<0,并达到平衡。HI的体积分数w(HI)随时间变化如下图(Ⅱ)所示,若改变反应条件,w(HI)的变化曲线如下图(Ⅰ)所示,则改变的条件可能是

A.恒温恒容条件下,加入适当催化剂
B.恒温条件下,缩小反应容器体积
C.恒容条件下,升高温度
D.恒温条件下,扩大反应容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知8gA能与32gB恰好反应,生成22gC和一定量D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量C,则D的摩尔质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质均易溶于水,分别按下列条件配成溶液,其中物质的量浓度最大的是
A.10mL5molL-1的A溶液加水配制成100mL溶液
B.9.2gB物质(式量为46)溶于水配成100mL溶液
C.1.806×1023个C的分子溶于水配成100mL溶液
D.0.1moLD物质溶于100mL2.5molL-1的D溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。下图是海水综合利用的部分流程图,据图回答问题:
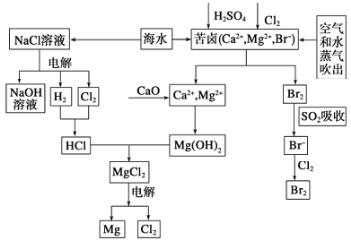
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式) ___________________。
(2)①电解饱和食盐水的化学反应方程式为______________。
②制取MgCl2的过程中涉及反应:MgCl2·6H2O![]() MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_______________。
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_______________。
(3)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,写出用SO2吸收发生的离子方程式_________,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为__________________。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是_____________;最后再用H2SO4处理得到Br2,之后加入CCl4进行Br2的萃取,最终用_____________方法得到单质Br2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备Na2CO3。下面是他的制备实验过程:
将50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:(I)用25mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;(II)小心煮沸溶液1~2分钟;(III)在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
(1)(II)中煮沸溶液的目的是 。
(III)中混合另一半NaOH溶液后发生的反应是 。(写离子方程式)
(2)按该同学的设计,第(I)步实验装置如下:
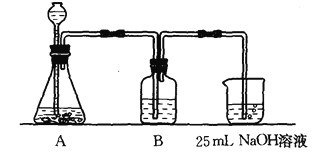
①装置A使用的试剂是 (固体)和 溶液;
②装置B使用的试剂最好是 (选择:水、饱和NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液),作用是 ;写出B中可能发生的离子方程式 ,如果不用B装置,最终得到的Na2CO3溶液中可能存在的杂质有 。
③有人认为实验步骤(II)、(III)的顺序对调,即先混合,再煮沸,更合理,你认为 (填“合理”或“不合理”)。原因为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com