
孔雀石的主要成分为Cu2(OH)2CO3,还含少量铁的氧化物和硅的氧化物。以下是实
验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:

(1)研磨孔雀石的目的是 。浸泡孔雀石的试剂A若选用过量的稀硫酸,则固体a是 (填化学式)。
(2)试剂B的目的是将溶液中的Fe2+转化为Fe3+,则试剂B宜选用 (填序号):
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
相应的离子方程式为: 。
(3)试剂C用于调节溶液pH,使Fe3+转化为沉淀予以分离。则试剂C宜选用 (填序号):
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
固体C的化学式为 。
(4)1 mol氨气通过加热的Cu2(OH)2 CO3可以产生1.5 mol金属铜,则该反应的化学方程式为 。
(5)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3 mol/L,必需将溶液调节至pH= 。
(1)(共4分)增大固体表面积(1分),以增大反应速率(1分)[类似意思均可]
SiO2(2分)
(2)(共4分)B(2分) 2Fe2++2H++H2O2=2Fe3++2H2O(2分)(未配平1分,写为化学方程式2FeSO4 + H2SO4 + H2O2 = Fe2(SO4)3 + 2H2O且正确1分)
(3)(共4分)D(2分) Fe(OH)3(2分)
(4)(共3分)3Cu2(OH)2CO3
+ 4NH3 6Cu
+ 3CO2 + 9H2O +2 N2(化学式1分、配平均1分,条件1分。)
6Cu
+ 3CO2 + 9H2O +2 N2(化学式1分、配平均1分,条件1分。)
(5)(共2分)2
【解析】
试题分析:(1)研磨孔雀石的目的是为了酸溶速率更快,所以答案为“增大固体接触面积,加快反应速率”,酸溶过程中不溶的固体为杂质SiO2。
(2)把Fe2+转化为Fe3+ 应该加入氧化剂,且不能带入杂质离子,所以用双氧水,选B。相应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O。
(3)因为目标产品是CuSO4·5H2O晶体,所以调节pH值使铁离子沉淀应选用的试剂不能带入杂质离子,所以选用固体CuO,所以沉淀物c为Fe(OH)3 和过量的CuO。
(4)碱式碳酸铜中通入氨气后有铜单质生成,说明铜被还原,NH3做还原剂。因为1mol氨气还原得到1.5mol铜单质,根据铜+2→0价,可知转移电子3mol,得失电子守恒,所以NH3失去电子也为3mol,所以可推测得NH3被氧化为了N2,所以可以得知其他产物还有CO2、H2O。所以列出反应物NH3+ Cu2(OH)2 CO3→Cu+
N2+CO2+H2O,然后根据氧化还原反应方程式配平得:3Cu2(OH)2CO3 + 4NH3 6Cu
+ 3CO2 + 9H2O +2 N2 。
6Cu
+ 3CO2 + 9H2O +2 N2 。
(5)根据Fe(OH)3溶解平衡Fe(OH)3
(s) 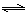 Fe3+
(aq)+3 OH- (aq)可得Ksp =c(
Fe3+ ) ·c3(OH- )= 1×10-39 ,所以把c(Fe3+)=1×10—3 mol/L带入公式中,计算得c(OH- )=
1×10-12 ,所以c(H+ )=Kw/ c(OH-
)= 10-2 ,所以pH=2。
Fe3+
(aq)+3 OH- (aq)可得Ksp =c(
Fe3+ ) ·c3(OH- )= 1×10-39 ,所以把c(Fe3+)=1×10—3 mol/L带入公式中,计算得c(OH- )=
1×10-12 ,所以c(H+ )=Kw/ c(OH-
)= 10-2 ,所以pH=2。
考点:本题考查的是化工生产流程题。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2011-2012学年江苏省上冈高级中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(14分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
| 物质 | pH (开始沉淀) | pH(完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省2012-2013学年高三12月月考化学试卷(解析版) 题型:选择题
孔雀石的主要成分为xCuCO3·yCu(OH)2·zH2O,为测定其中CuCO3的质量分数,称取a g样品进行实验。下列实验方案可行的是
A.充分加热样品,用碱石灰吸收逸出气体,增重b g
B.加热至样品质量不再发生变化,称得其质量为b g
C.向样品中加入足量的稀盐酸,用排水法收集逸出气体,得b mL气体
D.向样品中加入足量的稀盐酸,充分反应,将生成的气体全部通入到足量Ba(OH)2溶液中,过滤、洗涤、烘干,得b g固体
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省灵宝市高三上学期第三次质量检测化学试卷(解析版) 题型:实验题
孔雀石的主要成分为Cu2(OH)2CO3还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:

(1)试剂A的化学式是__________;操作I的名称是_________;操作Ⅱ用到的仪器有
酒精灯、玻璃棒、_________、坩埚钳和三角架。
(2)生成气体X的化学方程式为 。
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用_______(填选项序号)。
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
写出相应反应的离子方程式: 。
(4)已知

试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用 ___________(填选项序号);
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为_________。
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com